File word Đề thi vào 10 Chuyên Hóa Tỉnh Phú Yên – Năm học 2023 – 2024
File word Đề thi vào 10 Chuyên Hóa Tỉnh Phú Yên – Năm học 2023 – 2024
Câu 1. (2,0 điểm) Hãy chọn các chất tương ứng với các chữ cái để hoàn thành phương trình hoá học theo quá trình sau đây (điều kiện phản ứng phù hợp và mỗi chữ cái là một chất)
(1) A ® B + C + D (2) C + E ® G + H + I
(3) A + E ® K + G + I + H (4) K + H ® L + I + M
(5) L + H2SO4 ® N + H (6) K + H2SO4 ® N + E
Biết D, I và M là các đơn chất ở trạng thái khí trong điều kiện thường, khí I có tỉ khối so với SO2 là 1,1094. Để trung hoà dung dịch chứa 2,24 gam chất L cần 200 ml dung dịch H2SO4 0,1M.
Câu 2. (2,0 điểm) “Núi lửa Ijen (Kawahljen) cao 2.799 m so với mặt nước biển, thuộc quần thể núi lửa nằm gần thị trấn ven biển Banyuwangi, phía Đông đảo Java, là một trong số 76 ngọn núi lửa vẫn đang hoạt động ở Indonesia. Điểm độc đáo của núi lửa Ijen là vào khoảng 2 giờ đến 4 giờ (giờ sáng) mỗi ngày, ở xung quanh miệng núi lửa bạn có thể nhìn thấy hiện tưởng ngọn lửa màu xanh được ví von như những đốm lửa “ma trơi”, ngọn lửa xanh nổi tiếng thường chỉ xuất hiện vào sáng sớm, có thể cao đến 5,0 m và tắt rất nhanh trước bình minh
“Núi lửa Ijen (Kawahljen) cao 2.799 m so với mặt nước biển, thuộc quần thể núi lửa nằm gần thị trấn ven biển Banyuwangi, phía Đông đảo Java, là một trong số 76 ngọn núi lửa vẫn đang hoạt động ở Indonesia. Điểm độc đáo của núi lửa Ijen là vào khoảng 2 giờ đến 4 giờ (giờ sáng) mỗi ngày, ở xung quanh miệng núi lửa bạn có thể nhìn thấy hiện tưởng ngọn lửa màu xanh được ví von như những đốm lửa “ma trơi”, ngọn lửa xanh nổi tiếng thường chỉ xuất hiện vào sáng sớm, có thể cao đến 5,0 m và tắt rất nhanh trước bình minh
Tại miệng núi lửa này, hằng ngày có hàng trăm người công nhân thợ mỏ mạo hiểm cả tính mạng của mình để lấy những “khối vàng” chảy ra từ miệng núi lửa đang hoạt động với điều kiện làm việc vô cùng khắc nghiệt nhưng chỉ được trang bị những dụng cụ lao động vô cùng thô sơ. Thứ giúp bảo vệ họ trước những làn khói độc hại phun ra từ núi lửa chính là chiếc khẩu trang phòng độc, trong khi đó, trang phục của họ không có gì đặc biệt.”
Nội dung được in nghiêng nằm trong ngoặc kép được trích ra từ một số bài báo và tài liệu khoa học. Thí sinh đọc nội dung trên và trả lời các câu hỏi sau:
- “Khối vàng” được khai thác từ miệng núi lửa này có thành phần hoá học chính là chất gì? Ngọn lửa màu xanh ấy được phát ra từ phản ứng của những chất nào?
- Công nhân làm việc ở khu vực này có nguy cơ nhiễm độc bởi những hoá chất nào (liệt kê 4 chất có thể gây độc cho công nhân) và cho biết nguyên nhân vì sao tại khu vực miệng núi lửa đang hoạt động, thường tồn tại những hồ nước có tính axit rất cao?
Câu 3. (2,0 điểm) Hỗn hợp B gồm hai muối: M2CO3 và MHCO3. Chia 4,995 gam B thành ba phần bằng nhau:
– Phần 1: tác dụng hoàn toàn với dung dịch Ba(OH)2 dư, thu được 3,94 gam kết tủa.
– Phần 2: tác dụng hoàn toàn với dung dịch BaCl2 dư, thu được 0,985 gam kết tủa.
– Phần 3: phản ứng nhiều nhất với V ml dung dịch NaOH 0,1 M.
Tính giá trị của V.
Câu 4. (2,0 điểm) Cho 11,2 gam bột Fe vào dung dịch X chứa a mol Cu(NO3)2 và b mol Fe(NO3)3. Phản ứng hoàn toàn, thu được một kim loại và dung dịch Y có khối lượng bằng khối lượng dung dịch X ban đầu. Tính giá trị a, b. Biết dung dịch Y chỉ chứa một muối duy nhất và quá trình phản ứng, lượng nước bay hơi không đáng kể.
Câu 5. (2,0 điểm) Thực hiện phản ứng nhiệt nhôm với hỗn hợp Q gồm Al, CuO, Fe3O4 và Fe2O3 trong môi trường khí tro, thu được hỗn hợp chất rắn X. Cho hết lượng X vào dung dịch NaOH dư thu được dung dịch Y, chất không tan Z và 0,672 lít (đktc) khí H2. Dẫn dòng khí CO2 đến dư vào dung dịch chỉ chứa 16,2 gam muối sunfat và 2,464 lít (đktc) khí SO2 (sản phẩm khử duy nhất của axit H2SO4 đặc). Biết các phản ứng xảy ra hoàn toàn. Tính phần trăm khối lượng các chất trong Q.
Câu 6. (2,0 điểm) 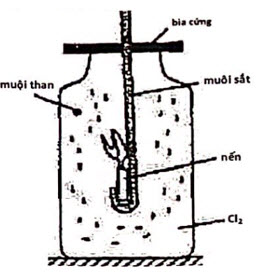 Học sinh A thực hiện thí nghiệm với các thao tác và kết quả như sau: Gắn một cây nến nhỏ vào muôi sắt sạch, đốt cháy nến và đưa vào bính chứa khí clo (xem hình). Nến tiếp tục cháy trong bình khí clo, màu khí clo nhạt dần, trong bình có nhiều muội than. Khi nến tắt, lấy muôi sắt ra, đưa mẩu giấy quì tím ẩm lên miệng bình, thấy mẩu giấy quỳ đổi màu. Học sinh A lại cho thêm một ít nước nguyên chất vào bình, lắc đều và tiếp tục nhỏ từ từ dung dịch NaOH vào bình, sau một thời gian, thấy có kết tủa xuất hiện ở dạng vết.
Học sinh A thực hiện thí nghiệm với các thao tác và kết quả như sau: Gắn một cây nến nhỏ vào muôi sắt sạch, đốt cháy nến và đưa vào bính chứa khí clo (xem hình). Nến tiếp tục cháy trong bình khí clo, màu khí clo nhạt dần, trong bình có nhiều muội than. Khi nến tắt, lấy muôi sắt ra, đưa mẩu giấy quì tím ẩm lên miệng bình, thấy mẩu giấy quỳ đổi màu. Học sinh A lại cho thêm một ít nước nguyên chất vào bình, lắc đều và tiếp tục nhỏ từ từ dung dịch NaOH vào bình, sau một thời gian, thấy có kết tủa xuất hiện ở dạng vết.
Đề xuất phương trình hoá học để làm cơ sở giải thích các hiện tượng thu được từ thí nghiệm mà học sinh A đã thao tác.
Câu 7. (2,0 điểm) Hỗn hợp khí X gồm một hidrocacbon no, mạch hở A (CnH2n+2), một hidrocacbon không no, mạch hở B (CmH2m) và hidro (H2). Cho 7,84 lít X qua chất xúc tác Ni, nung nóng, thu được 6,72 lít hỗn hợp khí Y. Dẫn toàn bộ lượng Y qua dung dịch KMnO4 dư, thấy màu tím của dung dịch bị nhạt một phần và khối lượng dung dịch sau phản ứng giảm 3,0 gam so với khối lượng dung dịch KMnO4 ban đầu. Sau phản ứng, khí Z ra khỏi dung dịch KMnO4 có thể tích 4,48 lít và có tỉ khối so với hidro là 20,25. Các khí cùng đo ở đktc, các phản ứng xảy ra hoàn toàn. Xác định công thức phân tử chất A, B và phần trăm thể tích của các khí có trong hỗn hợp Y.
Câu 8. (2,0 điểm) Trên thực tế, thành phần hoá học chính của khoáng pirit được coi là hỗn hợp của FeS2 và FeS. Khi xử lý hoàn toàn một mẫu khoáng pirit có thành phần xFeS2.yFeS (không chứa tạp chất) bằng lượng dư brom trong dung dịch KOH (quá trình xử lý không chịu tác động của oxi không khí và chất oxi hoá khác) thu được kết tủa đỏ nâu A và dung dịch B. Nung kết tủa A trong không khí đến khối lượng không đổi thu được 0,2 gam chất rắn. Thêm lượng dư dung dịch BaCl2 vào dung dịch B, thu được 1,1068 gam kết tủa trắng không tan trong môi trường axit.
Viết các phương trình hoá học đã xảy ra. Xác định tỉ lệ x: y (gần đúng, nguyên, tối giản) và tính khối lượng brom theo lí thuyết cần để oxi hoá mẫu khoáng.
Câu 9. (2,0 điểm) Dẫn chậm 3,36 lít (đktc) khí axetilen vào dung dịch HgSO4/H2SO4 loãng, đun nóng ở 800C một thời gian, thu được hỗn hợp Y (gồm hơi và khí). Cho toàn bộ Y phản ứng hết với một lượng dư dung dịch AgNO3/NH3 thu được 33,12 gam kết tủa.
- Viết các phương trình hoá học và tính phần trăm axetilen đã tham gia phản ứng cộng nước.
- Đề xuất cách thức để thu hồi lượng kim loại bạc có trong kết tủa sau phản ứng.
Câu 10. (2,0 điểm) Hỗn hợp X gồm hai axit hữu cơ no, có dạng RCOOH và R’(COOH)2, số nguyên tử cacbon trong axit một chức nhiều hơn số nguyên tử cacbon trong axit hai chức là 1 đơn vị.
Lấy m gam X cho tác dụng hết với kim loại Na, thu được 5,6 lít (đktc) khí H2. Ở một thí nghiệm khác, cũng m gam X được đốt cháy hoàn toàn bằng khí oxi dư, thu được 15,68 lít (đktc) khí CO2.
Xác định công thức cấu tạo các axit và tính giá trị m.
——————– HẾT- ——————-





