Đề thi vào 10 Chuyên Hóa Tỉnh Quảng Bình – Năm học 2020 – 2021
Đề thi vào 10 Chuyên Hóa Tỉnh Quảng Bình – Năm học 2020 – 2021
Câu 1. (2,0 điểm)
Nêu hiện tượng và viết phương trình hóa học của các phản ứng xảy ra (nếu có) khi:
- Cho Mg vào dung dịch CuSO
- Sục khí CO2 đến dư vào dung dịch NaAlO
- Cho rất từ từ đến dư dung dịch HCl vào dung dịch Na2CO
- Cho hỗn hợp gồm Na2O và Al2O3 (tỉ lệ số mol 1:1) vào nước dư.
- Sục khí etilen đến dư vào dung dịch Brom.
- Đun nóng chất béo (C17H35COO)3C3H5 với dung dịch NaOH.
- Cho dung dịch axit axetic đến dư vào mẫu đá vôi.
- Cho từ từ đến dư dung dịch Ba(OH)2 vào dung dịch NaHCO3.
Câu 2. (1,5 điểm)
1. Tiến hành thí nghiệm:
Đặt hai cốc trên hai đĩa cân. Rót dung dịch H2SO4 loãng vào hai cốc, lượng axit ở hai cốc bằng nhau, cân ở vị trí thăng bằng.
Cho mẫu Kẽm vào cốc thứ nhất và mẫu Sắt vào cốc thứ hai. Khối lượng của hai mẫu bằng nhau. Cân sẽ ở vị trí nào sau khi kết thúc phản ứng?
2. Bằng phương pháp hóa học, hãy phân biệt 5 lọ mất nhãn chứa 5 dung dịch:
NaCl; NH4Cl; FeCl3; AlCl3; (NH4)2SO4.
Câu 3. (1,5 điểm)
1. Viết các phương trình hóa học biểu diễn dãy chuyển đổi hóa học sau:
Tinh bột $\xrightarrow{(1)}$ glucozơ $\xrightarrow{(2)}$ rượu etylic $\xrightarrow{(3)}$ axit axetic $\xrightarrow{(4)}$etyl axetat
2. Có 4 chất hữu cơ X, Y, Z, T đều chứa 3 nguyên tố C, H, O và đều có tỉ khối hơi so với H2 là 30. Biết X tác dụng với Na và NaOH; Y, Z tác dụng với Na nhưng không tác dụng được với NaOH, H2; T không tác dụng với Na, NaOH.
Viết công thức cấu tạo X, Y, Z, T.
3. Cho 6,0 gam hỗn hợp gồm CH3COOH và CH3CH2CH2OH tác dụng vừa đủ với Na thu được khí E và m gam hỗn hợp muối F. Viết phương trình hóa học các phản ứng xảy ra và tính giá trị m.
Câu 4. (2,5 điểm)
1. Cho 27,4 gam Ba vào 400 gam dung dịch CuSO4 3,2 % thu được khí A, kết tủa B và dung dịch C.
Tính thể tích khí A (đktc).
Nung kết tủa B ở nhiệt độ cao đến khối lượng không đổi thì thu được bao nhiêu gam chất rắn?
Tính nồng độ phần trăm của chất tan trong dung dịch C.
| 2. Hòa tan hoàn toàn Al bằng V ml dung dịch H2SO4 1M và HCl 1M, thu được dung dịch Y chứa Al2(SO4)3, AlCl3 và H2SO4 dư. Cho từ từ đến dư dung dịch Ba(OH)2 vào Y, thấy khối lượng kết tủa tạo thành phụ thuộc vào số mol Ba(OH)2 theo đồ thị hình bên. Dựa vào đồ thị, hãy viết phương trình hóa học của các phản ứng xảy ra ứng với mỗi đoạn và tìm giá trị của y. | 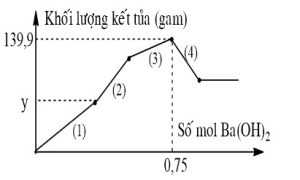 |
Câu 5. (2,5 điểm)
1. Hỗn hợp X gồm C3H8O3, C2H4O2, C3H6O3, CH2O. Đốt cháy hoàn toàn m gam hỗn hợp cần dùng vừa đủ V lit Oxi (đo ở đktc) thu được 44 gam CO2 và 19,8 gam H2O. Tính giá trị của V và m.
2. A là hỗn hợp gồm rượu etylic và 2 axit hữu cơ kế tiếp nhau có dạng CnH2n+1COOH và Cn+1H2n+3COOH. Cho $\frac{1}{2}$ hỗn hợp A tác dụng hết với Na thoát ra 3,92 lít H2 (đktc). Đốt cháy hoàn toàn $\frac{1}{2}$ hỗn hợp A, sản phẩm cháy được hấp thụ hết vào dung dịch Ba(OH)2 dư thì có 147,75 gam kết tủa và khối lượng bình Ba(OH)2 tăng 50,1gam.
a) Tìm công thức 2 axit trên.
b) Tính khối lượng các chất trong hỗn hợp A.
Cho: H=1; C=12; O=16; Zn= 65; Fe=56; Na=23; Ba=137; Cu=64; Al=27; S=32.





