File word Đề thi vào 10 Chuyên Hóa Quốc Học Huế – Năm học 2023 – 2024
File word Đề thi vào 10 Chuyên Hóa Quốc Học Huế – Năm học 2023 – 2024
Câu 1 (2,75 điểm)
Hãy xác định các chất A, A1, A2, … A9 trong sơ đồ dưới đây và viết các phương trình phản ứng hóa học xảy ra (ghi rõ điều kiện của phản ứng nếu có, mỗi mũi tên là một phản ứng).
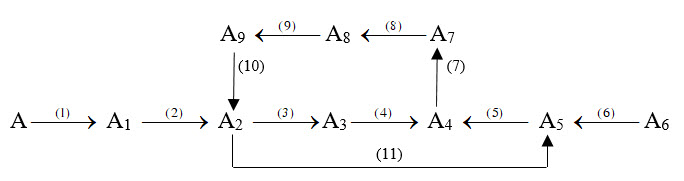
Biết rằng:
– A, A1, A2, … A9 là các hợp chất hữu cơ, trong đỏ A6, A7, A8 và A9 là những hiđrocacbon.
– Đốt cháy hoàn toàn 5,13 gam A thu được 7,92 gam CO2 và 2,97 gam H2O. Biết A có công thức phân tử trùng với công thức đơn giản nhất.
Một hỗn hợp X gồm Ba, Al, Fe, Cu và Ag. Hãy trình bày phương pháp hoá học để tách riêng từng kim loại (không làm thay đổi khối lượng của mỗi kim loại) ra khỏi hỗn hợp X. Viết các phương trình phản ứng hóa học xảy ra.
Câu 2 (2,25 điểm)
Một học sinh thực hiện thí nghiệm với các dung dịch sau: KOH, H2SO4 loãng, AgNO3, NaHCO3, NaOH loãng.
Thí nghiệm 1: Cho sản phẩm rắn thu được khi dẫn luồng khi H2 dư đi qua ống sứ đựng hỗn hợp gồm a mol CuO va a mol Al2O3, đun nóng vào dung dịch chứa 2a mol KOH.
Thí nghiệm 2: Cho hỗn hợp gồm a mol Cu và a mol Fe3O4 vào dung dịch chứa 4a mol H2SO4 loãng.
Thí nghiệm 3: Cho a mol Fe vào dung dịch chứa 2,5a mol AgNO3.
Thí nghiệm 4: Cho dung dịch chứa a mol Ba(OH)2 vào dung dịch chứa a mol NaHCO3.
Thí nghiệm 5: Nhỏ vài giọt dung dịch phenolphtalein vào cốc đựng dung dịch chứa a mol NaOH loãng, sau đó nhỏ từ từ đến hết dung dịch chứa a mol KHSO4 vào cốc và khuấy đều.
Các thí nghiệm phản ứng đều xảy ra hoàn toàn, có các nhận định sau:
(a) Có ba thí nghiệm mà dung dịch thu được chứa hai muối.
(b) Cho từ từ đến hết dung dịch chia 4a mol HCl vào dung dịch thu được sau thí nghiệm 1 thấy có kết tủa, sau đó kết tủa tan hoàn toàn.
(c) Dung dịch thu được sau khi thêm a mol KHSO4 ở thí nghiệm 5 có màu hồng.
(d) Trong các dung dịch tạo ra từ các thí nghiệm trên, chỉ có dung dịch ở thí nghiệm 4 làm thay đổi màu quỳ tím sang màu xanh.
Hãy cho biết nhận định nào đúng, nhận định nào không đúng. Giải thích vì sao? Viết các phương trình phản ứng hoá học xảy ra (nếu có).
Có bốn bình khí bị mất nhãn, mỗi bình chưa mỗi hỗn hợp khí sau: (C2H2, CO2), (C2H4, SO2), (CH4, C2H4), (H2, CO2). Bằng phương pháp hóa học, hãy nhận biết từng hỗn hợp khí chứa trong bốn bình trên. Viết các phương trình hỏa học xảy ra.
Câu 3 (2,5 điểm)
Đốt cháy hoàn toàn 1,24 gam hỗn hợp X gồm C2H2, C3H6 và C2H6, rồi hấp thụ toàn bộ sản phẩm cháy vào bình dụng 400 ml dung dịch Ca(OH)2 0,2M. Sau khi phản ứng kết thúc, thu được 7,0 gam kết . Mặt khác, cho 1,344 lit X (đktc) đi qua bình đựng dung dịch brom thì X làm mất màu tối đa 12 gam brom. Tính thành phần phần trăm theo thể tích của mỗi khí có trong hỗn hợp X.
Cho 6,44 gam hỗn hợp X gồm Na, Fe và Al vào nước lấy dư, thu được 1,792 lít khí (đktc) và chất rắn Y. Cho toàn bộ Y vào trong 150 ml dung dịch CuSO4 1M, thu được dung dịch Z và 7,68 gam một kim loại. Cho từ từ dung dịch NaOH loãng vào Z đến khi thu được lượng kết tủa lớn nhất, lọc kết tủa rồi đem nung trong không khí đến khối lượng không đổi, thu được m gam chất rắn T. Biết các phản ứng xảy ra hoàn toàn. Hãy tính thành phần phần trăm về khối lượng của mỗi kim loại có trong hỗn hợp X và tính m.
Câu 4 (2,5 điểm)
Hỗn hợp X gồm (RCOO)3C3H5 và RCOOH (R là gốc hiđrocacbon). Đun nóng hết 19,9 gam X với 200 ml dung dịch KOH 2M. Sau khi phản ứng xảy ra hoàn toàn, cô cạn dung dịch thu được 35,0 gam chất rắn khan. Mặt khác, đốt cháy hoàn toàn 19,9 gam X bằng lượng oxi vừa đủ thì thu được 33,0 gam CO2 và 11,7 gam H2O. Xác định công thức cấu tạo và tính thành phần phần trăm về khối lượng của các chất trong hỗn hợp X.
Hỗn hợp X gồm MgO, FeO, CuO, Fe2O3 và Fe3O4. Để hòa hoàn toàn m gam X thì cần dùng vừa đủ 100 ml dung dịch gồm HCl 2M và H2SO4 1M. Mặt khác, cho khí CO qua m gam X nung nóng, sau một thời gian thu được hỗn hợp rắn Y và hỗn hợp khí Z. Cho toàn bộ Z vào bình đựng 60 ml dung dịch Ca(OH)2 1M. đến khi phản ứng hoàn toàn thu được kết tủa và dung dịch T. Cho tiếp dung dịch Ba(OH)2 dư vào dung dịch T thấy kết tủa lại xuất hiện. Khi phản ứng kết thúc, tổng khối lượng hai lần kết tủa thu được là 12,895 gam. Cho toàn bộ chất rắn Y vào dung dịch H2SO4 đặc, nóng (dư), kết thúc phản ứng thu được 2,688 lít khi SO2 (đkc, sản phẩm khử duy nhất) và dung dịch chứa 30,4 gam muối, Tính m.
Cho biết nguyên tử khối (theo đvC) của các nguyên tố: H=1; O=16; N=14; C = 12; S=32; Br=80; Cl=35,5; Li=7; Na=23; K=39, Mg=24; Ca=40; Ba=137; Al=27; Zn=65; Fe=56; Pb=207; Cu =64; Ag = 108.
———HẾT———
Thí sinh không được sử dụng tài liệu. Cán bộ coi thì không giải thích gì thêm.





