Đề thi vào chuyên hóa Lâm Đồng – Năm học 2018 – 2019
Đề thi vào chuyên hóa Lâm Đồng – Năm học 2018 – 2019
Câu 1: (2.5 điểm)
- Nêu hiện tượng xảy ra và viết phương trình hóa học cho các trường hợp sau:
- Nhỏ từ từ dung dịch HCl vào dung dịch Na2CO3.
- Thêm từ từ dung dịch NaOH vào dung dịch AlCl3.
- Viết 03 phương trình hóa học khác nhau để điều chế Axit axetic.
Câu 2: (3.0 điểm)
- Chỉ dùng thuốc thử duy nhất là dung dịch bazơ, hãy nêu phương pháp nhận biết các chất hoặc dung dịch riêng biệt sau: Na2CO3, MgSO4, CH3COOH, C2H5OH, C6H6.
- Trình bày phương pháp hóa học nhận biết sự có mặt của các khí sau trong cùng một hỗn hợp: CO2, SO2, C2H4, CO.
Câu 3: (4.5 điểm)
- Cho sơ đồ sau:
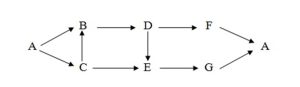
Biết A là kim loại; B, C, D, E, F, G là hợp chất của A. Xác định công thức của A, B, C, D, E, F, G và viết các phương trình hóa học xảy ra.
- Nêu phương pháp hóa học tinh chế rượu etylic có lẫn tạp chất là benzen.
- Nước thải của một nhà máy có pH < 7. Qua thí nghiệm, người ta thấy rằng cứ 5 lít nước thải cần dùng 1g Ca(OH)2 để trung hòa, mỗi giờ nhà máy thải ra 100.000 lít nước.
- Tính khối lượng Ca(OH)2 cần dùng để trung hòa lượng nước thải trong mỗi giờ.
- Tính khối lượng CaO cần dùng để trung hòa nước thải cho mỗi ngày. Biết nhà máy hoạt động 24 giờ/ngày.
Câu 4: (1.0 điểm)
Cho một ankan A ở thể khí. Để đốt cháy hoàn toàn 1,2 lít A cần dùng vừa hết 6 lít khí O2 lấy ở cùng điều kiện. Xác định công thức phân tử của A. Nếu cho A tác dụng với khí Cl2 ở 25oC có ánh sáng thì thu được bao nhiêu dẫn xuất monoclo của A.
Câu 5: (1.5 điểm)
Dùng một lượng dung dịch axit H2SO4 10% đun nóng để hòa tan vừa đủ 0,4 mol CuO. Sau phản ứng, làm nguội dung dịch thì thấy khối lượng CuSO4.5H2O tách ra khỏi dung dịch là 30 gam. Tính độ tan của CuSO4 trong điều kiện thí nghiệm trên.
Câu 6: (2.0 điểm)
Cho 23,8 gam hỗn hợp X (gồm Cu, Fe, Al) tác dụng vừa đủ với 14,56 lít khí Cl2 (đktc). Mặt khác cứ 0,25 mol hỗn hợp X tác dụng với dung dịch HCl dư thu được 0,2 mol khí (đktc). Tính thành phần phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp X.
Câu 7: (2.5 điểm)
Dẫn V lít hỗn hợp khí X (đktc) gồm C2H2 và H2 đi qua ống sứ đựng bột Ni nung nóng, thu được khí Y. Dẫn Y vào lượng dư AgNO3 trong dung dịch NH3 thu được 12 gam kết tủa. Khí đi ra khỏi dung dịch AgNO3/NH3 phản ứng vừa đủ với 16 gam Br2 và còn lại khí Z. Đốt cháy hoàn toàn khí Z thu được 2,24 lít khí CO2 (đktc) và 4,5 gam H2O. Tính V.
Câu 8: (3.0 điểm)
Đốt cháy hoàn toàn 84 gam hỗn hợp A gồm FeS2 và Cu2S bằng lượng khí O2 lấy dư ta được chất rắn B và 20,16 lít khí SO2 (đktc). Chuyển toàn bộ SO2 thành SO3 rồi hấp thụ vào nước được dung dịch C. Cho toàn bộ B vào C, khuấy kĩ cho các phản ứng xảy ra hoàn toàn, rồi lọc, rửa phần không tan nhiều lần bằng nước, thu được chất rắn D không tan. Tìm khối lượng của D.
(Cho biết: C = 12; H = 1; O = 16; Fe = 56; Cu = 64; Al = 27; S = 32; Cl = 35,5; Br = 80; Ag = 108; Ca = 40; N = 14)
Xem thêm: đề thi vào 10 Chuyên Hóa Lâm Đồng 2021





