Đề HSG Hóa 9 Đề thi vào 10 Chuyên Phú Thọ – Năm học 2020 – 2021
Đề HSG Hóa 9 Đề thi vào 10 Chuyên Phú Thọ – Năm học 2020 – 2021
Cho biết nguyên tử khối của các nguyên tố: H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24;
Al = 27; P = 31; S = 32; Cl = 35,5; K = 39; Ca = 40; Fe = 56; Cu = 64; Zn = 65; Br = 80; Ag = 108; Ba = 137
Câu 1. (2,0 điểm)
1. Nêu hiện tượng và viết các phương trình phản ứng xảy ra trong các trường hợp sau:
a) Sục khí etilen vào dung dịch Br2.
b) Cho dung dịch Na2CO3 vào dung dịch Fe2(SO4)3.
c) Cho KHSO4 vào dung dịch BaCl2.
d) Cho (NH4)2CO3 vào dung dịch nước vôi trong, đun nóng nhẹ.
2. Cho thí nghiệm được mô tả như hình vẽ sau:
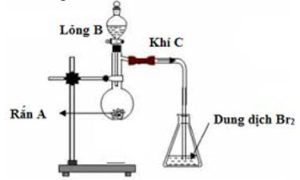
Biết sau khi phản ứng hoàn toàn thì dung dịch Br2 bị mất màu. A và B tương ứng có thể có các trường hợp sau: (1) Zn và dung dịch HCl; (2) Al4C3 và H2O; (3) FeS và dung dịch HCl; (4) CaCO3 và dung dịch HCl; (5) Na2SO3 và dung dịch H2SO4. Những trường hợp nào thỏa mãn thí nghiệm trên, viết các phương trình phản ứng xảy ra.
Câu 2. (2,0 điểm)
1. Bằng phương pháp hóa học, hãy nhận biết các chất rắn sau: tinh bột, xenlulozơ, saccarozơ, đá vôi và gluccozơ.
2. Cho các chất X, Y, Z, T (trong đó X, Y, Z đều là muối của natri) thỏa mãn các tính chất sau :
X hoặc Z tác dụng với dung dịch của chất Y đều thu được khí CO2.
X hoặc Y tác dụng với dung dịch của chất T đều thu được kết tủa trắng.
X hoặc T đều không phản ứng với dung dịch của chất Z.
Biết phân tử khối của các chất thỏa mãn: MX + MZ = 190; MX + MT = 365;
MZ + MT = 343; MT + MY = 379.
Xác định các chất X, Y, Z, T và viết các phương trình phản ứng minh họa.
Câu 3. (2,0 điểm)
1. Cho hỗn hợp X gồm Ba và Al. Cho m gam X vào nước dư, thu được 4,48 lít khí (ở đktc).
Cũng m gam X tác dụng với dung dịch NaOH dư, thu được 11,2 lít khí (ở đktc). Tính m.
2. Hỗn hợp X gồm Al, Fe, Mg. Cho m gam hỗn hợp X tác dụng với dung dịch HCl dư thu được dung
dịch Y. Cô cạn dung dịch Y thu được (m + 30,53) gam hỗn hợp muối khan. Oxi hóa hoàn toàn dung dịch Y cần 0,896 lít khí clo (ở đktc). Cho m gam hỗn hợp X tác dụng với oxi, sau 1 thời gian, thu được (m + 1,76) gam hỗn hợp Z. Cho Z tác dụng với dung dịch H2SO4 (đặc, nóng, dư), thu được V lít SO2 (ở đktc) và dung dịch T. Cô cạn dung dịch T thu được 57,1 gam muối khan.
Tính V và phần trăm khối lượng Fe trong hỗn hợp X ?
Câu 4. (2,0 điểm)
1. Đốt cháy hoàn toàn m gam photpho bằng oxi dư rồi hòa tan sản phẩm vào nước dư thu được dung
dịch X. Cho 0,5 mol KOH vào dung dịch X, cô cạn dung dịch sau phản ứng thu được $\frac{\text{193m}}{\text{31}}$ gam chất rắn khan. Biết các phản ứng xảy ra hoàn toàn. Tính m.
2. Cho 11,56 gam hỗn hợp A gồm 3 muối FeCl3, BaBr2, KCl tác dụng với 440 ml dung dịch AgNO3 0,5M thu được dung dịch D và kết tủa B. Lọc kết tủa B, cho 0,15 mol bột Fe vào dung dịch D thu được chất rắn T và dung dịch E. Cho T vào dung dịch HCl loãng dư tạo ra 2,128 lít H2 (ở đktc) và còn phần chất không tan. Cho dung dịch KOH dư vào dung dịch E thu được kết tủa, nung kết tủa trong không khí đến khối lượng không đổi thu được 6,8 gam chất rắn. Biết các phản ứng xảy ra hoàn toàn.
a) Viết các phương trình phản ứng xảy ra
b) Tính khối lượng kết tủa B.
Câu 5. (2,0 điểm)
1. Cho 6,9 gam rượu etylic và a gam axit axetic vào một bình cầu. Thêm tiếp axit sunfuric đặc vào. Đun
sôi hỗn hợp trong bình cầu một thời gian, thu được 0,08 mol este và dung dịch X. Chia X thành 2 phần bằng nhau.
Cho dung dịch BaCl2 dư vào phần 1 thu được 29,125 gam kết tủa.
Để trung hòa hết phần 2, cần tối đa 270 ml dung dịch KOH 1M.
Tính a.
2. Trong một bình kín chứa hỗn hợp gồm hidrocacbon X mạch hở (thể khí ở điều kiện thường) và
0,06 mol O2 (lấy dư), bật tia lửa điện để đốt cháy hoàn toàn X. Cho toàn bộ hỗn hợp sau phản ứng đi qua bình đựng 3,5 lít dung dịch Ca(OH)2 0,01M, thu được 3 gam kết tủa và thoát ra một khí duy nhất có thể tích 0,224 lít (ở đktc). Biết các phản ứng xảy ra hoàn toàn, nước bị ngưng tụ khi cho qua dung dịch.
Xác định công thức phân tử của X.
………………..Hết………………………
Có thể bạn quan tâm: Đề Chuyên Hóa Tuyên Quang 2021





