Đề thi vào 10 Chuyên Hóa Tỉnh Quảng Trị – Năm học 2020 – 2021
Đề thi vào 10 Chuyên Hóa Tỉnh Quảng Trị – Năm học 2020 – 2021
Câu 1: (1,25 điểm)
1) Viết các phương trình hóa học để hoàn thành sơ đồ chuyển hóa dưới đây và ghi rõ điều kiện của phản ứng (nếu có). Mỗi mũi tên tương ứng với một phương trinh hóa học.
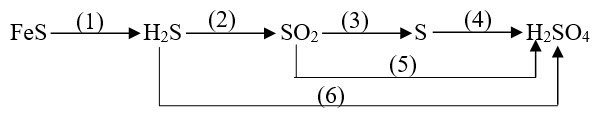
2) Chỉ dùng thêm phenolphtalein, hãy trình bày cách nhận biết các dung dịch H2SO4, HCI, Ba(OH)2, AlCl3, Na2SO4 bằng phương pháp hóa học. Viết phương trình hóa học của các phản ứng xảy ra.
Câu 2: (1,0 điểm)
1) Hãy nêu hiện tượng và viết phương trình hóa học của các phản ứng xảy ra khi tiến hành các thí nghiệm sau:
a) Cho một mẫu kim loại Na vào dung địch FcCl3.
b) Cho dung địch axit axctic vào dung dịch Na2SiO3.
2) Khí oxi đóng một vai trò rất quan trọng đối với đời sống và hoạt động sản xuất của con người nên việc tìm hiểu các phản ứng điều chế oxi là rất cần thiết. Hãy viết các phương trình tạo ra khí oxi trực tiếp từ các chất sau: KCIO3, KMnO4, H2O, CO2 và ghi rõ điều kiện (nếu có).
Câu 3: (1,0 điểm)
1. Trình bày phương pháp hóa học để tách từng chất khí CH4. C2H4, C2H2 ra khỏi hỗn hợp của chúng. Viết phương trình hóa học của các phản ứng xảy ra.
2. Có thể điều chế trực tiếp được axit axetic bằng một phản ứng hóa học từ các chất nào trong số các chất: ancol etylic, sacarozơ, ancol metylic, butan, etyl axetat, glyxerol? Viết các phương trình hóa học minh họa.
Câu 4: (1,0 điểm)
Poli(metyl mctacrylat) còn có tên gọi khác là thủy tinh hữu cơ Plexiglass, thường được sử dụng để làm kính ô-tô. Khi có va đập, loại kinh này vỡ thành các hạt vụn ít sắc cạnh nên sẽ an toàn hơn cho người tham gia giao thông. Biết rằng công thức cấu tạo thu gọn của poli(metyl metacrylat) là:
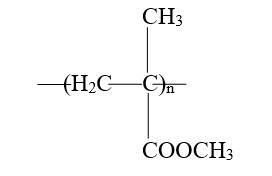
Để điều chế poli(metyl metacrylat), người ta tiến hành phản ứng trùng hợp chất hữu cơ X ở điều kiện thích hợp. Chất X được tổng hợp bằng phản ứng trực tiếp giữa X1 và X2; trong đó X1 tác dụng được với kim loại Na và muối CaCO3. X2 không tác dụng được với muối CaCO3 nhưng tác dụng được với kim loại Na.
a) Viết công thức cấu tạo thu gọn của X, X1, X2 và phương trình hóa học các phản ứng xảy ra.
b) Viết phương trình hóa học của các phản ứng xảy ra (nếu có) giữa X với H2 (Ni, t0), HBr, dung dịch Br2, dung dịch NaOH.
Câu 5: (1,5 điểm)
1) Hòa tan hoàn toàn 14,3 gam muối ngậm nước có công thức hóa học Na2CO3.nH2O vào 185,7 gam nước, thu được dung dịch muối nồng độ 2,65%. Xác định giá trị của n.
2) Một mẫu quặng pyrotuzit có thành phần chính là MnO2 và lẫn tạp chất CaCO3. Hòa tan hoàn toàn 8,96 gam quặng pyrotuzit bằng một lượng dư HCI đặc thu được hỗn hợp khí A gồm clo và cacbonic, tỉ khối của A so với hiđro bằng 32,8. Xác định thành phần phần trăm về khối lượng của MnO2 trong mẫu quặng trên.
3) Hòa tan hỗn hợp gồm 2,7 gam Al và 5,1 gam Al2O3 vào cốc chứa 200 ml dung dịch H2SO4 2M thu được dung dịch X. Thêm tiếp 64,26 gam BaO vào dung dịch X, sau khi các phản ứng xảy ra hoàn toàn thì tiến hành lọc kết tủa rồi đem nung đến khối lượng không đổi thu được a gam chất rắn. Viết các phương trình hóa học của phản ứng xảy ra và tính giá trị của a.
Câu 6: (1,0 điểm)
Hấp thụ hoàn toàn 0,112 lít khí Cl2 (đktc) vào 100 ml dung dịch NaI 0,25M. Sau khi phản ứng xảy ra hoàn toàn, đun nóng dung dịch để đuổi hết I2 rồi tiếp tục thêm nước vào để được dung dịch có thể tích 100 ml (dung dịch B).
a) Tính nồng độ mol/l của mỗi muối trong dung dịch B.
b) Thêm từ từ đến hết V lít dung dịch AgNO3 0,05M vào dung dịch B thu được m gam kết tủa. Tính giá trị của V khi:
(1) Trường hợp 1: m = 1,175.
(2) Trường hợp 2: m = 4,386.
Giả thiết rằng AgI kết tủa trước, sau đó AgI kết tủa hết thì mới đến AgCl kết tủa.
Câu 7: (0,75 điểm)
Hỗn hợp X gồm 0,1 mol C2H2 và 0,2 mol H2. Dẫn X đi qua bề mặt xúc tác Ni ở nhiệt độ thích hợp thu được hỗn hợp khí Y gồm C2H2, C2H4, C2H6 và H2. Tỉ khối của Y so với hiđro là 7,5.
a) Tính số mol H2 đã tham gia phản ứng.
b) Dẫn Y đi qua bình chứa một lượng dư dung dịch Br2, sau khi các phản ứng xảy ra hoàn toàn thấy có m (gam) Br2 đã tham gia phản ứng và còn lại V lít khí Z (đktc) không bị hấp thụ. Tính giá trị của m và V, biết rằng khối lượng bình chứa dung dịch Br2 sau phản ứng tăng thêm 1,6 gam so với ban đầu.
Câu 8: (0,75 điểm)
Đốt cháy hoàn toàn một hợp chất hữu cơ X bằng oxi thu được CO2 và H2O. Khi hóa hơi 2,9 gam X thu được thể tích hơi đúng bằng thể tích của 1,4 gam khí N2 ở cùng điều kiện nhiệt độ, áp suất. Viết các công thức cấu tạo thu gọ có thể có của X.
Câu 9: (1,0 điểm)
Hỗn hợp X gồm kim loại Cu và một oxit sắt có công thức FexOy. Hòa tan hoàn toàn 15,68 gam X bằng một lượng dư H2SO4 đặc, nóng thu được dung dịch Y (chỉ chứa muối sunfat của kim loại, axit dư, nước) và khí SO2. Hấp thụ toàn bộ khí SO2 bằng 500 ml dung dịch Ba(OH)2 0,2M thu được 17,37 gam kết tủa.
a) Xác định công thức hóa học của FexOy, biết rằng cô cạn dung dịch Y thu được 40,0 gam hỗn hợp muối khan.
b) Cho 7,84 gam X ở trên vào cốc chứa 160 ml dung dịch HCl 1M thu được dung dịch P và m1 gam chất rắn Q không tan. Cho dung dịch P tác dụng với 400,0 gam dung dịch AgNO3 8,5% thu được m2 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn, tính giá trị m1, m2.
Câu 10: (0,75 điểm)
Đốt cháy hoàn toàn 73,8 gam hỗn hợp X gồm axit panmitic (C15H31COOH), axit stearic (C17H35COOH) và các chất béo tạo bởi hai axit đó bằng oxi thu được 4,7 mol CO2 và 81,72 gam H2O. Mặt khác, khi cho 73,8 gam X tác dụng vừa đủ với 130 ml dung dịch KOH 2M thu được dung dịch Y. Toàn bộ lượng muối khan trong dung dịch Y được dùng làm một loại xà phòng, trong đó muối kali của axit béo chiếm 90% về khối lượng. Tính khối lượng xà phòng thu được.
……………………. HẾT ………………….





