Đề thi HSG Hóa 9 – Hà Nội – Năm học 2018 – 2019
Đề thi HSG Hóa 9 – Hà Nội – Năm học 2018 – 2019
Bài I (3,25 điểm)
1. Hãy trả lời đầy đủ 8 câu hỏi tương ứng với 8 hàng ngang. Tìm từ hàng ngang phù hợp và xác định từ hàng dọc?
Hàng 1 : Phản ứng của $\mathrm{Fe}$ với dung dịch $\mathrm{HCl}$ thuộc loại phản ứng hóa học nào ?
Hàng 2 : Trong phản ứng của sắt với khí oxi thì vai trò của oxi là chất gì ?
Hàng 3 : Tên loại muối được tạo ra từ phản ứng giữa axit sunfuhiđric và kiềm dư.
Hàng 4 : Các hợp chất $\mathrm{Zn}(\mathrm{OH})_{2}, \mathrm{Fe}(\mathrm{OH})_{3}, \mathrm{NaOH}$..đều thuộc loại hợp chất hóa học nào ?
Hàng 5 : Tên hóa học của chất trong đời sống có tên gọi là diêm sinh.
Hàng 6 : Hạt vi mô gồm hạt nhân mang điện tích dương và vỏ tạo bởi một hay nhiều electron mang điện tích âm được gọi là gì ?
Hàng 7 : Khi điện phân hỗn hợp nóng chảy của nhôm oxit và chất $A$ thu được nhôm và oxi. Tên gọi của chất $\mathrm{A}$ là gì ?
Hàng 8 : Chất được tạo nên từ một nguyên tố hóa học gọi là gì ?
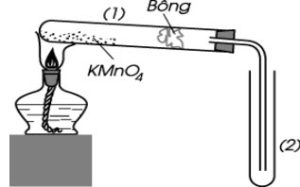
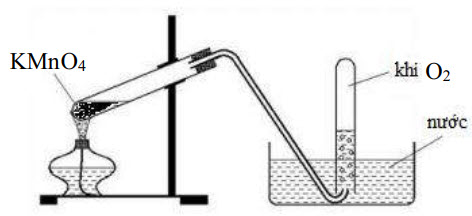
2. Cho hình vẽ mô tả quá trình điều chế khí oxi trong phòng thí nghiệm. Giải thích các cách làm sau :
a) ống nghiệm (2) đặt thẳng đứng và miệng ống quay lên trên.
b) đun tập trung ngọn lửa ở phần đáy ống nghiệm (1).
c) đặt một ít bông trong ống nghiệm (1).
Bài II (3,75 diêm)
1. Cho các chất $X, Y, Z, T$ (trong đó $X, Y, Z$ đều là muối của natri) thỏa mãn các tính chất sau :
– X hoặc Z tác dụng với dung dịch của chất $Y$ đều thu được khí $\mathrm{CO}_{2}$.
– X hoặc Y Yác dụng với dung dịch của chất $\mathrm{T}$ đều thu được kết tủa trắng.
– X hoặc T đều không phản ứng với dung dịch của chất $Z$.
Biết phân tử khối các chất thỏa mãn :
$$
\mathrm{M}_{\mathrm{X}}+\mathrm{M}_{\mathrm{Z}}=190 ; \mathrm{M}_{\mathrm{X}}+\mathrm{M}_{\mathrm{T}}=365 ; \mathrm{M}_{\mathrm{Z}}+\mathrm{M}_{\mathrm{T}}=343 ; \mathrm{M}_{\mathrm{T}}+\mathrm{M}_{\mathrm{Y}}=379 .
$$
Xác định các chất $X, Y, Z, T$ và viết phương trình hóa học minh họa.
2. Hợp chất $\mathrm{A}$ có công thức hóa học là $\mathrm{MX}_{2}$, trong đó $\mathrm{M}$ chiếm $51,282 \%$ về khối lượng. Phân tử $\mathrm{A}$ có tổng số hạt proton là 38 . Trong nguyên tử nguyên tố $\mathrm{M}$, số hạt proton bằng số hạt nơtron; trong nguyên tử nguyên tố X số hạt nơtron nhiều hơn số hạt proton là 1 . Tìm số hạt proton của $\mathrm{M}$ và $\mathrm{X}$.
Bài III (4,5 điểm)
1. Chia 32,5 gam muối sunfua của kim loại $M$ làm hai phần. Đốt cháy hoàn toàn phần 1 trong khí oxi dư thu được sản phẩm khí $\mathrm{A}$ có mùi hắc. Phần 2 tác dụng hết với dung dịch $\mathrm{HCl}$ thu được khí $\mathrm{B}$ có mùi trứng thối. Cho toàn bộ lượng khí $\mathrm{A}$ và lượng khí $\mathrm{B}$ tác dụng với nhau (hiệu suất phản ứng là 95\%) thu được 18,24 gam kết tủa màu vàng, phần khí thoát ra cho tác dụng với dung dịch $\mathrm{CuSO}_{4}$ dư (hiệu suất phản ứng 100\%) thu được 6,72 gam kết tủa màu đen.
a) Viết phương trình hóa học xảy ra.
b) Xác định tên kim loại $M$.
2. Cho $\mathrm{m}$ gam hỗn hợp $\mathrm{X}$ gồm $\mathrm{Na}_{2} \mathrm{CO}_{3}, \mathrm{MgO}$, a mol Fe $\mathrm{F}_{4}$ và $2 \mathrm{a}$ mol $\mathrm{KHCO}_{3}$ vào 400 gam dung dịch $\mathrm{H}_{2} \mathrm{SO}_{4} 17,15 \%$. Sau khi các phản ứng xảy ra hoàn toàn thu được khí $\mathrm{CO}_{2}$; dung dịch chứa $(\mathrm{m}+42,68)$ gam muối sunfat trung hòa và 345,44 gam nước. Tìm giá trị của $\mathrm{m}$ và $\mathrm{a}$.
Bài IV (3,25 điểm)
1. Hợp chất $X$ là oxit của photpho, trong đó photpho chiếm $43,66 \%$ về khối lượng. Xác định công thức hóa học của $X$ và hoàn thành sơ đồ chuyển hóa sau :
$$
\mathrm{X} \stackrel{+\mathrm{H}_{2} \mathrm{O}}{\longrightarrow} \mathrm{Y} \stackrel{+\mathrm{NaOH} \mathrm{du}}{\longrightarrow} \mathrm{Z} \stackrel{+\mathrm{AgNO}_{3}}{\longrightarrow} \mathrm{T}
$$
Biết : $Y, Z$ và $T$ là những hợp chất khác nhau và đều chứa photpho.
2. Nhỏ rất từ từ dung dịch $\mathrm{Ba}(\mathrm{OH})_{2} 1 \mathrm{M}$ vào dung dịch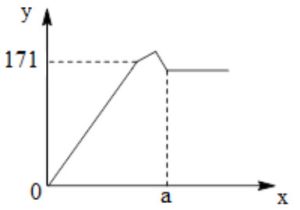
a) Giải thích hình dạng của đồ thị bằng phương trình hóa học.
b) Tìm giá trị của $\mathrm{a}$.
Bài V (5,25 điểm)
1. Cho hơi nước đi qua than nóng đỏ xảy ra hai phản ứng hóa học sau :
$$
\begin{aligned}
& \mathrm{C}+\mathrm{H}_{2} \mathrm{O} \longrightarrow \mathrm{CO}+\mathrm{H}_{2} \\
& \mathrm{C}+2 \mathrm{H}_{2} \mathrm{O} \longrightarrow \mathrm{CO}_{2}+2 \mathrm{H}_{2}
\end{aligned}
$$
Sau phản ứng, thu được $\mathrm{V}$ lít (đktc) hỗn hợp $\mathrm{X}$ gồm $\mathrm{CO}, \mathrm{CO}_{2}$ và $\mathrm{H}_{2}$. Dẫn $\mathrm{X}$ qua dung dịch $\mathrm{Ca}(\mathrm{OH})_{2}$ thấy thoát ra hỗn hợp khí $\mathrm{Y}$ gồm $\mathrm{CO}$ và $\mathrm{H}_{2}$; đồng thời thu được 2 gam kết tủa ; khối lượng dung dịch sau phản ứng giảm 0,68 gam so với khối lượng dung dịch $\mathrm{Ca}(\mathrm{OH})_{2}$ ban đầu. Biết $\mathrm{Y}$ có tỉ khối so với $\mathrm{H}_{2}$ là 3,6. Tìm giá trị của $\mathrm{V}$.
2. Hoà tan hoàn toàn 6,3175 gam hỗn hợp muối gồm $\mathrm{NaCl}, \mathrm{KCl}, \mathrm{MgCl}_{2}$ vào nước rồi thêm vào đó 100 $\mathrm{ml}$ dung dịch $\mathrm{AgNO}_{3}$ 1,2M. Sau phản ứng lọc tách kết tủa $\mathrm{X}$ thu được dung dịch $\mathrm{Y}$. Cho 2 gam $\mathrm{Mg}$ vào dung dịch $\mathrm{Y}$ đến khi phản ứng kết thúc thu được kết tủa $\mathrm{Z}$ và dung dịch $\mathrm{T}$. Cho kết tủa $\mathrm{Z}$ tác dụng với dung dịch $\mathrm{HCl}$ dư, sau phản ứng thấy khối lượng của $\mathrm{Z}$ giảm 1,844 gam. Thêm $\mathrm{NaOH}$ dư vào dung dịch $\mathrm{T}$, lọc lấy kết tủa đem nung đến khối lượng không đổi thu được 0,3 gam chất rắn $\mathrm{E}$. Tính khối lượng các kết tủa $\mathrm{X}, \mathrm{Z}$ và phần trăm khối lượng các muối có trong hỗn hợp ban đầu.
Cho : $\mathrm{H}=1 ; \mathrm{C}=12 ; \mathrm{N}=14 ; \mathrm{O}=16 ; \mathrm{Na}=23 ; \mathrm{Mg}=24 ; \mathrm{Al}=27 ; \mathrm{P}=31 ; \mathrm{S}=32 ; \mathrm{Cl}=35,5 ; \mathrm{K}=39$;
$$
\mathrm{Ca}=40 ; \mathrm{Fe}=56 ; \mathrm{Ag}=108 ; \mathrm{Ba}=137 .
$$
-Hết