Đề thi vào 10 Chuyên Hóa LHP Nam Định – Năm học 2020 – 2021
Đề thi vào 10 Chuyên Hóa LHP Nam Định – Năm học 2020 – 2021
Cho: H = 1; C = 12; O = 16; Cl = 35,5; S = 32; Na = 23; Mg = 24; Al = 27; Fe = 56; Cu = 64.
Câu 1: (3,0 điểm)
1) Cho các nhận định sau:
a/ Các hạt cấu tạo nên hầu hết các hạt nhân nguyên tử là proton, notron và electron.
b/ Khối lượng nguyên tử tập trung ở hạt nhân nguyên tử.
2) Các nhận định trên có chính xác không ? Giải thích ngắn gọn.
Nguyên tử nguyên tố X có tổng số hạt proton, electron, notron là 52. Trong hạt nhân nguyên tử X, số hạt mang điện ít hơn số hạt không mang điện là 1.
a/ Xác định số electron của nguyên tố X.
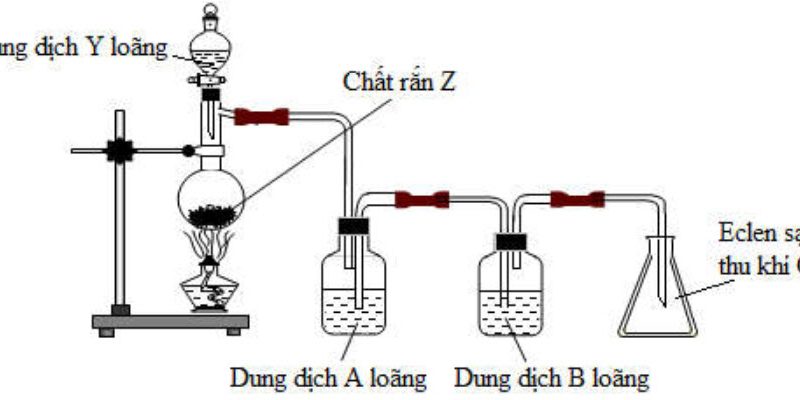
Sơ đồ dưới đây mô tả thí nghiệm điều chế khí X trong phòng thí nghiệm.
b/ Gọi tên X, cho biết chất (1) trong bình cầu có thể là chất nào ?
c/ Viết một phương trình hóa học của phản ứng xảy ra trong bình cầu ?
d/ Khí Cl2 sinh ra thường lẫn tạp chất là HCl và hơi nước. Nêu vai trò bình đựng dung dịch NaCl bão hòa và dung dịch H2SO4 đặc.
3/ Cho 40 gam Fe nguyên chất vào 416 ml dung dịch H2SO4 15% có khối lượng riêng 1,10 g/cm3. Hỗn hợp được lắc đến khi phản ứng xảy ra hoàn toàn. Lọc dung dịch thu được, chuyển vào bình nón, axit hóa bằng vài giọt dung dịch axit H2SO4 và làm lạnh đến nhiệt độ phòng. Bình nón được hàn kín và để trong hai ngày. Sau đó, tiến hành lọc hỗn hợp, phần dung dịch thu được cho bay hơi một nửa khối lượng trong khí quyển CO2 và để kết tinh ở 20 0C trong bình hàn kín. Ngày hôm sau, lấy tinh thể rửa với cồn và làm khô nhanh trong giấy lọc. Kết quả thu được 140 gam tinh thể màu xanh, chứa 11,51% khối lượng lưu huỳnh.
a/ Viết phương trình hóa học của phản ứng chính và cho biết công thức của phân tử của tinh thể trong quá trình thí nghiệm trên.
b/ Có thể thay dung dịch H2SO4 15% bằng dung dịch H2SO4 60% để tăng tốc độ phản ứng không ? Tại sao cần để dung dịch bay hơi trong khí quyển CO2 ? Điều gì xảy ra nếu cho dung dịch bay hơi trong không khí ? Giải thích và viết các phương trình hóa học kèm theo.
c/ Tính hiệu suất tạo thành tinh thể, biết dung dịch bão hòa ở 20 0C chứa 78% khối lượng nước.
d/ Một hỗn hợp axit HNO3 đặc và H2SO4 được thêm vào dung dịch của sản phẩm trên, sau khi phản ứng xảy ra hoàn toàn, thấy có khí màu nâu đỏ thoát ra. Sau đó, cho hỗn hợp sản phẩm bay hơi đến khi dung dịch trở nên sền sệt, tiến hành làm lạnh, xuất hiện tinh thể màu vàng chứa 17,08% khối lượng lưu huỳnh. Cho biết công thức phân từ của tinh thể và viết phương trinh hóa học cùa phàn ứng xảy ra.
Cân 2 (2,0 điểm).
1) Trình bày hiện tượng và viết phương trinh hóa học của phàn ứng xảy ra khi:
a/ Cho từ từ đến dư khí CO2 vào dung dịch Ca(OH)2.
b/ Dung dịch CaCl2 tác dụng với dung dịch NaHCO3, đun nóng.
2) Giải thích các hiện tượng sau:
a/ Trong tự nhiên, nước ở một số vùng là nước cứng tam thời, là nước có chứa các muối axit như: Ca(HCO3)2, Mg(HCO3)2. Ở những vùng này, khi đun nước lâu ngày thấy xuất hiện lớp cặn dưới đáy ấm.
b/ Để quả mau chín, người ta thường xếp quả xanh và quả chín gần nhau.
3) CO là một chất khí không màu, rất độc. Khi khí CO đi vào cơ thể theo đường hô hấp thì nó sẽ chiếm vị trí của O2 trong Hemoglobin dẫn đến giảm chức năng vận chuyển oxi cùa máu. Khí CO phản ứng với khí Cl2 theo tl lệ 1:1 khi có mặt ánh sáng thu được khí X (cực độc) dùng trong chiến tranh thế giới thứ nhất.
a/ Đề xuất công thức cấu tạo của X, biết rằng trong X hóa trị cùa cacbon là IV, hóa trị của oxi là II, hóa trị của clo là I.
b/ Viết phương trinh phản ứng xảy ra khi cho X tác dụng với dung dịch NaOH, biết rằng thu được hai muối là Na2CO3 và NaCl.
4) Khi cho hơi nước qua than nung đỏ, người ta thu được hỗn hợp khí Y gồm H2, CO vả CO2. Dẫn 1 mol khí Y (ở đktc) qua CuO dư, nung nóng thi khối lượng chất rắn giảm 14,4 gam và thu được hỗn hợp Z gồm hơi nước và CO2. Dẫn Z vào nước vôi trong dư, thu được m gam kết tùa.
Viết các phương trinh phản ứng xảy ra và tính m. Biết các phàn ứng xảy ra hoàn toàn.
Câu 3 (1,5 điểm).
1) Bậc cùa cacbon là số nguyên tử cacbon liên kết trực tiếp với nguyên tứ cacbon đang xét. Ví dụ: phân tử propan có công thức cấu tạo CH3-CH2-CH3 có hai nguyên tử cacbon bậc I ở hai đầu và một nguyên tử cacbon bậc II ớ giữa. Hiđrocacbon X mạch hở trong đó các nguyên tử chỉ liên kết với nhau bằng liên kết đơn. Trong phân tử X có 1 nguyên từ cacbon bậc III, một nguyên tử cacbon bậc II và còn lại là các nguyên tứ cacbon bậc 1.
a/ Xác định công thức cấu tạo cùa X.
b/ Tương tự như khi cho metan (CH4) tác dụng với khí Clo (có mặt ánh sáng), các nguyên tứ hiđro trong X có thể lần lượt bị thế bởi các nguyên tử clo.
i) Khi cho X với Cl2 theo tỉ lệ mol 1:1 có mặt ánh sáng thi thu được tối đa bao nhiêu sản phẩm hữu cơ? Viết công thức cấu tạo cùa các sản phẩm đó.
ii) Viết một phương trinh phản ứng của X với Cl2 theo ti lệ mol 1 : 1.
2) Brom là chất lỏng tan ít trong nước và tan tốt trong dung môi hữu cơ. Cho vào ống nghiệm 2 ml dung dịch nước brom (có mâu đỏ nâu). Nhỏ từ từ vào ổng nghiệm đó 1 ml benzen. Trong ống nghiệm có 2 lớp chất lỏng, lớp dưới có thể tích lớn hơn và có màu đỏ nâu, lớp chắt lỏng phía trên có màu vàng.
a/ Giải thích hiện tượng trên.
b/ Lấy đũa thủy tinh khuấy đều để hai lớp chất lỏng trộn lẫn vào nhau, sau đó để yên ống nghiệm. Dự đoán hiện tượng xảy ra và giải thích.
3) Cho hidrocacbon Y mạch hở thể khí ở điều kiện thường. Đốt chảy hoàn toàn mẫu hiđrocacbon này ở 127 °C vả 1 atm trong khí oxi dư thấy thế tích hỗn hợp khí không thay đổi sau phản ứmg. Xác định công thức cấu tạo có thể có của Y. Biết nước bay hơi ở nhiệt độ 100°C và áp suất 1 atm.
Câu 4 (1.5 điểm).
1) Trước khi tiêm, thầy thuốc thường dùng bông tấm cồn (dung dịch rượu etylic) xoa lên da bệnh nhân để sát trùng chỗ tiêm.
a/ Thực nghiệm cho thấy cồn 750 có tác dụng sát trùng hiệu quả nhất. Giải thích điều này.
b/ Cần bao nhiêu mL nước đề pha chế được 1 lít cồn 75° từ cổn 950.
Thủy phân hoàn toàn một lượng khoai tây chứa 20% tinh bột, đem toàn bộ lượng C6H12O6 lên men, khí sinh ra phản ứng tối đa với 60,2 ml dung dịch NaOH 30% (khối lượng riêng 1,33 g/mL).
a/ Viết phương trình hóa học của các phản ứng xảy ra, ghi rõ điều kiện thực hiện chuyển hóa.
b/ Tính khối lượng khoai tây đã dùng. Biết hiệu suất chung của cả quá trình là 80%.
2) Chất X có công thức phân tứ CnH2nO2 (phân tử chứa một nhóm -COOH), tinh chất hóa học tương tự axit axetic và chất Y có công thức phàn từ CnH2nO2 (phân tử chứa một nhóm -OH), tính chất hóa học tương tự rượu etylic. Cho m gam hỗn hợp E gồm X và Y tác dụng với Na dư, thu được 1,568 lit khí H2 (ở đktc). Đốt cháy hoàn toàn m gam hỗn hợp E thu được 6,272 lít khí CO2 (ở đktc) và 6,48 gam nước. Mặt khác, thêm một ít dung dịch H2SO4 đặc (làm xúc tác) vào m gam hỗn hợp E và đun nhẹ thu được 3,96 gam chất hữu cơ F.
a/ Xác định công thức phân tứ của X. Y.
b/ Tính hiệu suất cùa phản ứng tạo thành F.
Câu 5 (2.0 điểm).
1/ Biến thiên entanpi của phản ứng hóa học được tính bằng tổng entanpi của các chất sản phẩm trừ tổng entanpi của các chất phản ứng, mỗi giá trị entanpi nhân với hệ số tương ứng trong phương trinh hóa học. Entanpi của các đơn chất ở trạng thái chuẩn bằng 0.
Có 3 hiđrocacbon X. Y, Z chưa biết đều có 2 nguyên cacbon trong phân tử. Số nguyên tử hidro trong các phân tử tăng dần theo thứ tự X < Y < Z. Entanpi tạo thành chuẩn (kí hiệu $\Delta H_{S}^{0}$) của các hiđrocacbon và CO2, H2O được cho ở bảng sau:
| Chất | X | Y | Z | CO2 (khí) | H2O (k) |
| $\Delta H_{S}^{0}$ (kJ/mol) | 227 | 52 | -85 | -395 | -242 |
a/ Viết công thức cấu tạo và gọi tên cùa X, Y, Z. Viết phương trinh điều chế X, Y (chỉ bằng một phản ứng) dùng các hóa chất thông dụng trong phòng thí nghiệm.
b/ Viết phương trinh cháy hoàn toàn của 3 hiđrocacbon với hệ số nguyên tối giản. Tính biến thiên entanpi cùa mỗi phản ứng cháy trong điều kiện chuẩn.
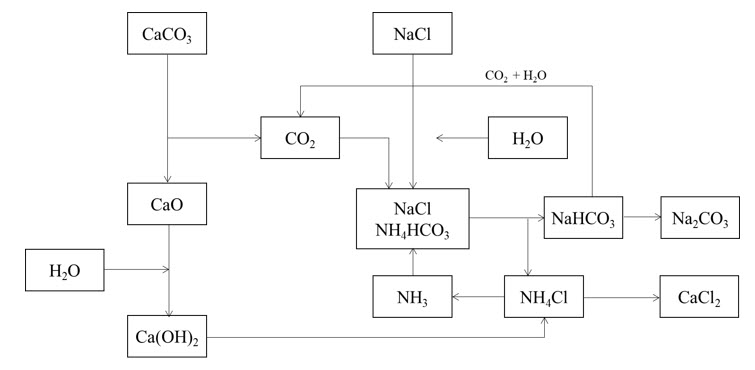
2) Sơ đồ dưới đây mô tả quá trình Solvay, để điều chế Na2CO3 trong công nghiệp.
Dựa vào sơ đồ trên, hãy:
a/ Viết phương trình của phản ứng tổng quát tạo Na2CO3.
b/ Viết phương trình cân bằng của cặp muối NaCl/NH4HCO3.
c/ Viết phương trình hình thành NH4HCO3.
d/ Nêu vai trò của Ca(OH)2 và viết phương trình phản ứng.
– HẾT –