Đề thi HSG Hóa 9 – Hà Nội – Năm học 2019 – 2020
Đề thi HSG Hóa 9 – Hà Nội – Năm học 2019 – 2020
Bài I (4,0 điểm)
1. Cho sơ đồ thí nghiệm điều chế khí clo như sau:
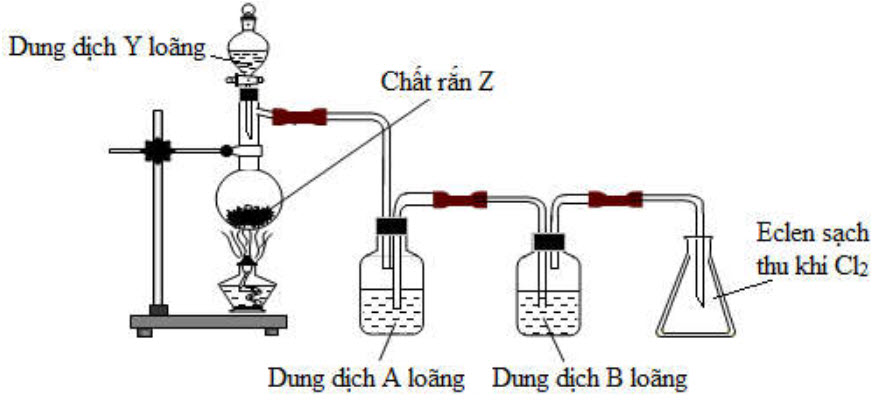
a) Trong sơ đồ thí nghiệm trên có những điểm nào chưa chính xác, giải thích tại sao?
b) Khi sơ đồ thí nghiệm là đúng, chỉ rõ các chất $\mathrm{Y}, \mathrm{Z}, \mathrm{A}, \mathrm{B}$ và viết phương trình hóa học xảy ra.
2. Tại sao khi bón phân ure hoặc phân đạm amoni không nên bón cùng với vôi?
3. Nêu hiện tượng, giải thích và viết phương trình hóa học cho các thí nghiệm sau:
a) Nhỏ 1 – 2 ml dung dịch axit clohiđric vào ống nghiệm đựng một ít bột sắt (III) oxit, lắc nhẹ.
b) Nhỏ từ từ đến dư dung dịch natri hiđroxit vào ống nghiệm đựng dung dịch nhôm clorua.
c) Cho dung dịch bari hiđroxit vào ống nghiệm đựng dung dịch amoni sunfat, đun nóng nhẹ.
Bài II (4,0 điểm)
1. Nguyên tử của nguyên tố $X$ có tổng số hạt proton, nơtron, electron là 60 . Trong hạt nhân nguyên tử của nguyên tố $X$ có số hạt mang điện bằng số hạt không mang điện. Số hạt mang điện trong nguyên tử của nguyên tố $Y$ ít hơn số hạt mang điện trong nguyên tử của nguyên tử nguyên tố $X$ là 6 .
a) Xác định tên các nguyên tố X, Y.
b) Viết phương trình hóa học tương ứng với các nguyên tố $X, Y$ theo sơ đồ chuyển hóa sau:
$$
\mathrm{X} \rightarrow \mathrm{XO} \rightarrow \mathrm{X}(\mathrm{OH})_{2} \rightarrow \mathrm{XCO}_{3} \rightarrow \mathrm{X}\left(\mathrm{HCO}_{3}\right)_{2} \rightarrow \mathrm{XY}_{2} \rightarrow \mathrm{NaY} \rightarrow \mathrm{Y}_{2} \rightarrow \mathrm{Br}_{2}
$$
2. Có 4 lọ hóa chất mất nhãn được kí hiệu là $\mathrm{A}, \mathrm{B}, \mathrm{C}, \mathrm{D}$. Mỗi lọ đựng một trong các dung dịch sau: $\mathrm{HCl}$, $\mathrm{NaHSO}_{4}, \mathrm{BaCl}_{2}, \mathrm{NaHSO}_{3}$. Để xác định hóa chất đựng trong mỗi lọ, người ta tiến hành các thí nghiệm và thấy hiện tượng như sau:
– Cho dung dịch ở lọ $\mathrm{A}$ vào dung dịch ở lọ $\mathrm{B}$ thấy xuất hiện kết tủa;
– Cho dung dịch ở lọ $\mathrm{B}$ hay lọ $\mathrm{D}$ vào dung dịch ở lọ $\mathrm{C}$ đều thấy có bọt khí không màu có khả năng làm mất màu cánh hoa;
– Cho dung dịch ở lọ $\mathrm{D}$ vào dung dịch ở lọ $\mathrm{A}$ thì không thấy hiện tượng gì.
Hãy biện luận để xác định hóa chất đựng trong các lọ A, B, C, D. Viết phương trình hóa học của các phản ứng xảy ra.
Bài III (4,0 điểm)
1. Cho hỗn hợp bột $\mathrm{Cu}$ và $\mathrm{CuO}$ với tỉ lệ mol tương ứng là $2: 3$ tan hoàn toàn trong dung dịch $\mathrm{H}_{2} \mathrm{SO}_{4} 94 \%$, thu được khí $\mathrm{SO}_{2}$ duy nhất và dung dịch $\mathrm{X}$. Trong dung dịch $\mathrm{X}$, nồng độ phần trăm của muối đồng và của axit dư bằng nhau. Giả xử nước bay hơi không đáng kể. Xác định nồng độ phần trăm của muối đồng trong dung dịch $X$.
2. Cho hỗn hợp $\mathrm{A}$ gồm $\mathrm{x}$ mol $\mathrm{FeS}_{2}$ và $\mathrm{y}$ mol $\mathrm{Cu}_{2} \mathrm{~S}$ tác dụng hết với dung dịch $\mathrm{HNO}_{3}$ loãng, vừa đủ, đun nóng thu được khí NO duy nhất và dung dịch chỉ chứa muối sunfat của các kim loại. Xác định giá trị của tỉ lệ $x: y$.
Bài IV (4,0 điểm)
1. Hòa tan hoàn toàn $\mathrm{m}$ gam hỗn hợp $\mathrm{X}$ gồm $\mathrm{Na}, \mathrm{Na}_{2} \mathrm{O}, \mathrm{NaOH}, \mathrm{Na}_{2} \mathrm{CO}_{3}$ bằng dung dịch $\mathrm{H}_{2} \mathrm{SO}_{4} 20 \%$ vừa đủ, thu được 0,896 lít hỗn hợp khí $Y$ có tỉ khối so với $\mathrm{H}_{2}$ là 16,75 và dung dịch $\mathrm{Z}$ có nồng độ 25,725\% (giả xử nước bay hơi không đáng kể). Cô cạn dung dịch $\mathrm{Z}$, thu được 8,52 gam muối khan. Tìm giá trị của m.
2. Cho 0,765 gam hỗn hợp $\mathrm{Al}$ và $\mathrm{Mg}$ tan hoàn toàn trong $160 \mathrm{ml}$ dung dịch $\mathrm{H}_{2} \mathrm{SO}_{4} 0,25 \mathrm{M}$, thu được dung dịch $\mathrm{X}$ và khí $\mathrm{H}_{2}$. Cho $340 \mathrm{ml}$ dung dịch $\mathrm{NaOH} 0,25 \mathrm{M}$ vào dung dịch $\mathrm{X}$, sau khi các phản ứng xảy ra hoàn toàn thu được 1,65 gam kết tủa gồm 2 chất. Mặt khác, cho từ từ dung dịch chứa hỗn hợp KOH $0,8 \mathrm{M}$ và $\mathrm{Ba}(\mathrm{OH})_{2} 0,1 \mathrm{M}$ vào $\mathrm{X}$ đến khi thu được lượng kết tủa lớn nhất, lọc lấy kết tủa đem nung đến khối lượng không đổi, thu được $\mathrm{m}$ gam chất rắn. Tìm giá trị của $\mathrm{m}$.
Bài V (4,0 điểm)
1. Trong thực tế người ta thường đốt bột lưu huỳnh tạo ra khí $\mathrm{X}$ để xông cho đông dược, trái cây nhằm bảo quản được lâu hơn.
a) Giải thích cách làm trên.
b) Hấp thụ hoàn toàn a gam khí X vào $200 \mathrm{ml}$ dung dịch $\mathrm{NaOH} \mathrm{b} \mathrm{M}$ thu được dung dịch Y. Chia Yäàm hai phần bằng nhau:
– Phần 1: cho tác dụng với dung dịch $\mathrm{CaCl}_{2}$ dư thấy xuất hiện $\mathrm{c}$ gam kết tủa;
– Phần 2: cho tác dụng với dung dịch nước vôi trong dư thấy xuất hiện d gam kết tủa.
Biết $\mathrm{d}>\mathrm{c}$, tìm biểu thức quan hệ giữa $a$ và $b$.
2. Nung nóng 4,48 gam Fe trong 1,4 lít (đktc) hỗn hợp khí $\mathrm{X}$ gồm $\mathrm{Cl}_{2}$ và $\mathrm{O}_{2}$ thu được 7,065 gam hỗn hợp $\mathrm{Y}$ chỉ gồm các oxit và muối clorua (không còn khí dư). Hòa tan hoàn toàn $\mathrm{Y}$ bằng dung dịch $\mathrm{HCl}$ vừa đủ, thu được dung dịch $\mathrm{Z}$. Cho $\mathrm{AgNO}_{3}$ tới dư vào dung dịch $\mathrm{Z}$, thu được $\mathrm{m}$ gam kết tủa gồm $\mathrm{AgCl}$ và $\mathrm{Ag}$. Tìm giá trị của $\mathrm{m}$.