Đề thi HSG Hóa 9 – Tỉnh Hải Dương – Năm học 2021 – 2022
Đề thi HSG Hóa 9 – Tỉnh Hải Dương – Năm học 2021 – 2022
Câu I. (2,0 điểm)
1) Cho hỗn hợp $\mathrm{X}$ gồm $\mathrm{Fe}_{2} \mathrm{O}_{3}, \mathrm{MgO}, \mathrm{Zn}$, $\mathrm{Cu}$ tác dụng với dung dịch $\mathrm{HCl}$ dư thu được dung dịch $\mathrm{Y}$, khí $\mathrm{Z}$ và chất rắn $\mathrm{A}$. Hòa tan $\mathrm{A}$ trong dung dịch $\mathrm{H}_{2} \mathrm{SO}_{4}$ đặc, nóng, dư thu được khí $\mathrm{B}$ (sản phẩm khử duy nhất). Sục từ từ khí $\mathrm{B}$ vào dung dịch nước vôi trong dư, thu được kết tủa $\mathrm{D}$. Cho từ từ dung dịch $\mathrm{NaOH}$ vào dung dịch Y cho đến khi kết tủa không đổi, thu được chất rắn E. Nung $E$ trong không khí đến khối lượng không đổi thu được chất rắn $\mathrm{G}$. Biết các phản ứng xảy ra hoàn toàn. Xác định thành phần các chất có trong $\mathrm{Y}, \mathrm{Z}, \mathrm{A}, \mathrm{B}$, $\mathrm{E}, \mathrm{D}, \mathrm{G}$ và viết các phương trình phản ứng xảy ra.
2) Nêu hiện tượng, viết các phương trình phản ứng xảy ra trong các thí nghiệm sau
a. Thêm từ từ đến dư dung dịch $\mathrm{NaOH}$ vào dung dịch gồm $\mathrm{HCl}$ và $\mathrm{AlCl}_{3}$.
b. Cho dung dịch $\mathrm{HCl}$ từ từ tới dư vào dung dịch $\mathrm{Na}_{2} \mathrm{CO}_{3}$.
c. Cho mẩu $\mathrm{Na}$ vào dung dịch $\mathrm{CuSO}_{4}$.
d. Sục khí $\mathrm{SO}_{2}$ từ từ đến dư vào dung dịch $\mathrm{Ba}(\mathrm{OH})_{2}$.
Câu II. (2,0 điểm)
1) Cho 5 lọ hóa chất mất nhãn, mỗi lọ đựng một trong các dung dịch chất sau: $\mathrm{NaOH}, \mathrm{NaCl}, \mathrm{HCl}_{2} \mathrm{H}_{2} \mathrm{SO}_{4}$, $\mathrm{BaCl}_{2}$. Chỉ dùng thêm phenolphtalein, trình bày phương pháp hóa học để nhận biết dung dịch ở mỗi lọ và viết các phương trình phản ứng xảy ra nếu có.
2) Muối ăn thường có lẫn các tạp chất sau: $\mathrm{Na}_{2} \mathrm{SO}_{4}, \mathrm{MgSO}_{4}, \mathrm{MgCl}_{2}, \mathrm{CaCl}_{2}$. Trình bày phương pháp hóa học loại bỏ các tạp chất có trong muối ăn để thu được $\mathrm{NaCl}$ tinh khiết và viết các phương trình phản ứng xảy ra.
Câu III. (2,0 điểm)
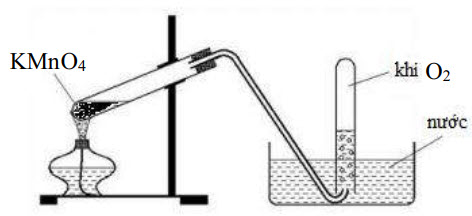
1) Hình vẽ sau mô tả cách lắp dụng cụ điều chế oxi trong phòng thí nghiệm bằng cách nhiệt phân $\mathrm{KMnO}_{4}$ ở dạng rắn:
a. Cách lắp bộ dụng cụ thí nghiệm điều chế oxi như hình vẽ ở trên đúng hay sai? Giải thích và nêu cách lắp dụng cụ đúng nhất.
b. Phương pháp thu khí ở trên dựa vào tính chất nào của oxi?
c. Khi kết thúc thí nghiệm, tại sao phải tháo ống dẫn khí ra trước khi tắt đèn cồn?
d. Nếu lấy các chất $\mathrm{KMnO}_{4}$ và $\mathrm{KClO}_{3}$ có khối lượng bằng nhau thì khi nhiệt phân hoàn toàn chất nào điều chế được lượng oxi nhiều hơn. Hãy giải thích bằng cách tính toán trên cơ sở phương trình hóa học.
2) Hỗn hợp $\mathrm{X}$ gồm $\mathrm{SO}_{2}$ và $\mathrm{O}_{2}$ có tỉ khối so với hidro là 25,6 . Cho $\mathrm{V}$ lít hỗn hợp $\mathrm{X}$ (ở đktc) vào một bình kín có xúc tác thích hợp, đun nóng bình một thời gian, thu được hỗn hợp Y có tỉ khối so với hidro là 31,22. Cho Y tác dụng với $280 \mathrm{~mL}$ dung dịch $\mathrm{Ba}(\mathrm{OH})_{2} 1 \mathrm{M}$, sau khi phản ứng hoàn toàn thu được 59,3 gam kết tủa, dung dịch $\mathrm{Q}$ (chỉ chứa một chất tan) và khí thoát ra không làm mất màu nước brom. Các khí không tan và không tác dụng với nước. Xác định hiệu suất phản ứng tổng hợp $\mathrm{SO}_{3}$ và tính giá trị của $\mathrm{V}$.
Câu IV. (2,0 điểm)
1. Cho hỗn hợp rắn $\mathrm{X}$ có khối lượng $\mathrm{m}$ gam gồm $\mathrm{KHCO}_{3}, \mathrm{CaCO}_{3}$. Nung hỗn hợp $\mathrm{X}$ trong không khí đến khối lượng không đổi, sau phản ứng thu được hỗn hợp chất rắn $\mathrm{Y}$. Cho $\mathrm{Y}$ vào nước dư, thu được dung dịch $\mathrm{Z}$ và $0,2 \mathrm{~m}$ gam chất rắn không tan. Cho dung dịch $\mathrm{HCl} 1 \mathrm{M}$ từ từ vào dung dịch $\mathrm{Z}$ đến khi có khí bắt đầu thoát ra thì vừa hết $\mathrm{V}_{1}$ lít dung dịch $\mathrm{HCl}$, còn đến khi khí thoát ra vừa hết thì hết $\mathrm{V}_{2}$ lít dung dịch $\mathrm{HCl}$. Biết khí sinh ra không tan, không tác dụng với nước.Viết các phương trình phản ứng xảy ra và xác định tỉ lệ $\frac{\mathrm{V}_{1}}{\mathrm{~V}_{2}}$
2) Hòa tan hoàn toàn 7,2 gam $\mathrm{Mg}$ bằng 73,5 gam dung dịch $\mathrm{H}_{2} \mathrm{SO}_{4} 80 \%$ (axit đặc), sau phản ứng thu được dung dịch $\mathrm{X}$. Cho $700 \mathrm{~mL}$ dung dịch $\mathrm{NaOH} 1 \mathrm{M}$ vào dung dịch $\mathrm{X}$, lọc kết tủa thu được dung dịch Y. Cô cạn dung dịch $\mathrm{Y}$ đến khi chất rắn thu được có khối lượng không đổi thì thu được 49,08 gam chất rắn khan. Biết sản phẩm khử của $\mathrm{H}_{2} \mathrm{SO}_{4}$ là $\mathrm{S}$ và $\mathrm{SO}_{2}$, nước không bị bay hơi trong quá trình phản ứng, các phản ứng xảy ra hoàn toàn, khí sinh ra không tan và không tác dụng với nước.
Xác định nồng độ phần trăm của $\mathrm{MgSO}_{4}$ trong dung dịch $\mathrm{X}$.
Câu V. (2,0 điểm)
1) Nung nóng 40,3 gam hỗn hợp chất rắn $\mathrm{A}$ gồm $\mathrm{KClO}_{3}$ và $\mathrm{KMnO}_{4}$ một thời gian thu được hỗn hợp chất rắn $\mathrm{B}$ và khí $\mathrm{O}_{2}$. Cho $\mathrm{B}$ tác dụng hết với dung dịch $\mathrm{HCl}$ đặc, dư và đun nóng, sau phản ứng thu được 14,56 lít khí clo. Trộn lượng oxi thu được với không khí theo tỉ lệ thể tích 1:3 trong một bình kín thu được hỗn hợp khí X. Cho vào bình một lượng cacbon rồi đốt cháy hết cacbon, thu được hỗn hợp khí $\mathrm{Y}$ gồm 3 khí có tỉ khối so với hidro là 14,96. Cho $\mathrm{Y}$ tác dụng với dung dịch $\mathrm{Ca}(\mathrm{OH})_{2}$ dư, sau phản ứng thu được 6,0 gam kết tủa. Biết các khí đo ở đktc, trong không khí nitơ chiếm $80 \%$ về thể tích, còn lại là oxi.
a. Viết các phương trình phản ứng xảy ra.
b. Tính \% khối lượng mỗi chất trong $\mathrm{A}$ và số $\mathrm{mol} \mathrm{HCl}$ đã phản ứng.
2) Nung $\mathrm{m}$ gam hỗn hợp gồm $\mathrm{Al}$ và $\mathrm{Fe}_{\mathrm{x}} \mathrm{O}_{\mathrm{y}}$ trong điều kiện không có không khí, sau phản ứng thu được rắn $\mathrm{B}$. Chia $\mathrm{B}$ thành 2 phần
+ Cho phần một tác dụng với dung dịch $\mathrm{NaOH}$ dư, thu được 1,12 lít khí và 8,4 gam chất rắn không tan
+ Cho phần hai tác dụng với dung dịch $\mathrm{H}_{2} \mathrm{SO}_{4}$ đặc, nóng dư thu được 12,32 lít $\mathrm{SO}_{2}$ (sản phẩm khử duy ổịât) và dung dịch $\mathrm{D}$ có chứa 117,0 gam hỗn hợp muối sunfat trung hòa. Biết các phản ứng xảy ra hoàn toàn, chất khí đo ở đktc).
a. Viết các phương trình phản ứng xảy ra.
b. Xác định giá trị $\mathrm{m}$ và công thức $\mathrm{Fe}_{\mathrm{x}} \mathrm{O}_{\mathrm{y}}$.
Cho biết nguyên tư khối của các nguyên tố: $H=1 ; L i=7 ; B e=9 ; C=12 ; O=16 ; N a=23 ; M g=24 ; A l=27$; $S=32 ; \mathrm{K}=39 ; \mathrm{Ca}=40 ; \mathrm{Mn}=55 ; \mathrm{Fe}=56 ; \mathrm{Cu}=64 ; \mathrm{Zn}=65 ; \mathrm{Rb}=85,5 ; \mathrm{Ba}=137$;