File word Đề thi HSG Hóa 9 – Bắc Giang – Năm học 2022 – 2023
File word Đề thi HSG Hóa 9 – Bắc Giang – Năm học 2022 – 2023
I. PHẦN TRẮC NGHIỆM (6,0 điểm)
Câu 1: Hidrocacbon $\mathrm{X}$ mạch hở có công thức phân từ $\mathrm{C}_{4} \mathrm{H}_{\mathrm{n}}$, biết $\mathrm{X}$ không tạo kết tủa khi tác dụng với dung dịch $\mathrm{AgNO}_{3} / \mathrm{NH}_{3}$ dưr. Số công thức cấu tạo phủ hợp với $\mathrm{X}$ là:
A. 7
B. 11
C. 9
D. 8
Hướng dẫn
$\mathrm{CH}_{3} \mathrm{CH}_{2} \mathrm{CH}_{2} \mathrm{CH}_{3}, \mathrm{CH}_{3} \mathrm{CH}\left(\mathrm{CH}_{3}\right)_{2}, \mathrm{CH}_{2}=\mathrm{CHCH}_{2} \mathrm{CH}_{3}, \mathrm{CH}_{3} \mathrm{CH}=\mathrm{CHCH}_{3}, \mathrm{CH}_{2}=\mathrm{C}\left(\mathrm{CH}_{3}\right)_{2}, \mathrm{CH}_{3} \mathrm{C} \equiv \mathrm{CCH}_{3}$ $\mathrm{CH}_{2}=\mathrm{C}=\mathrm{CHCH}_{3}, \mathrm{CH}_{2}=\mathrm{CH}-\mathrm{CH}=\mathrm{CH}_{2}$
Câu 2: Thực hiện các thi nghiệm sau:
(1) Suc khi $\mathrm{CO}_{2}$ dư vào dung dịch $\mathrm{Ca}(\mathrm{OH})_{2}$
(2) Đun nóng dung dịch $\mathrm{Mg}\left(\mathrm{HCO}_{3}\right)_{2}$
(3) Cho dung dịch $\mathrm{Ba}\left(\mathrm{HCO}_{3}\right)_{2}$ vào dung dịch $\mathrm{Ca}(\mathrm{OH})_{2}$
(3) Cho dung dịch $\mathrm{Fe}\left(\mathrm{NO}_{3}\right)_{2}$ vào dung dịch $\mathrm{AgNO}_{3}$
(5) Cho dung dịch $\mathrm{Ba}(\mathrm{OH})_{2}$ dư vào dung dịch $\mathrm{Al}_{2}\left(\mathrm{SO}_{4}\right)_{3}$
Sau khi các phản ứng xảy ra hoàn toàn, số thí nghiệm có xuất hiện kết tủa là:
A. 2
B. 4
C. 3
D. 5
Hương dẫn
Thí nghię̧m (2), (3), (4), (5)
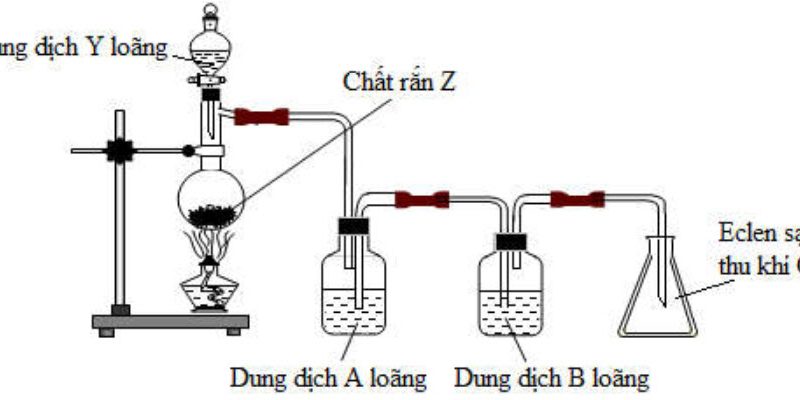
Câu 3: Trong phòng thi nghiệm, khi $\mathrm{X}$ được điều chế và thu vảo bình tam giác bằng cách đẩy nưởc như hình:
Phản ứng nào sau đây không áp dụng được cách thu khí như trên:
A. $\mathrm{Zn}+2 \mathrm{HCl} \rightarrow \mathrm{ZnCl}_{2}$
B. $\mathrm{NaCl}+\mathrm{H}_{2} \mathrm{SO}_{4} \rightarrow \mathrm{NaHSO}_{4}+\mathrm{HCl}$
C. $2 \mathrm{KClO}_{3} \rightarrow 2 \mathrm{KCl}+3 \mathrm{O}_{2}$
D. $\mathrm{CH}_{3} \mathrm{COONa}+\mathrm{NaOH} \stackrel{\mathrm{Can}^{\circ}}{\longrightarrow} \mathrm{CH}_{4}+\mathrm{Na}_{2} \mathrm{CO}_{3}$
Câu 4: Hòa tan 32,8 gam hổn hợp các muối $\mathrm{NaCl}, \mathrm{NaNO}_{3}, \mathrm{MgCl}_{2}, \mathrm{Mg}\left(\mathrm{NO}_{3}\right)_{2}$ vào nước được dung dịch $\mathrm{X}$ chứa 4 ion, trong đó số $\mathrm{mol}^{2}$ ion $\mathrm{NO}_{3}{ }^{*}$ bằng 1,5 lần số $\mathrm{mol}$ ion $\mathrm{Mg}^{2+}$. Dung dịch $\mathrm{X}$ phản úng được tối đa với $0,4 \mathrm{~mol}$ $\mathrm{NaOH}$ trong dung dịch. Cho $\mathrm{X}$ tác dụng với dung dịch $\mathrm{AgNO}_{3}$ dư, thu được $\mathrm{m}$ gam kết tủa. Giá trị của $\mathrm{m}$ là:
A. 14,35
B. 28,70
C. 57,40
D. 43,05
Hướng dẫn
Câu 5: Cho phản ứng hạt nhân: ${ }_{90}^{232} \mathrm{Th} \rightarrow{ }_{82}^{308} \mathrm{~Pb}+\mathrm{x}_{2}^{4} \mathrm{He}+\mathrm{y}_{-1}^{0} \mathrm{e}$. Giá trị của y là:
A. 4
B. 8
C. 2
D. 6
Hướng dẫn
BT số khối : $232=208+4 \mathrm{x}$ và $\mathrm{BTĐT}: 90=82+2 \mathrm{x}-\mathrm{y} \rightarrow \mathrm{x}=6$ và $\mathrm{y}=4 \rightarrow \mathrm{A}$
Câu 6 : Cho 18,3 gam hỗn họp gồm $\mathrm{Ba}$ và $\mathrm{Na}$ vào 1 lit dung dịch $\mathrm{CuSO}_{4} 0,5 \mathrm{M}$ sau khi các phản ứng xáy ra hoàn toản, thu được $\mathrm{m}$ gam kết tủa và 4,48 lit khí $\mathrm{H}_{2}$ (dktc). Giá trị của $\mathrm{m}$ là:
A. 45,5
B. 42,9
C. 40,5
D. 50,8
Hướng dẵn
$\left|\begin{array}{l}\mathrm{Ba}^{2} \\ \mathrm{Na}^{\mathrm{b}}\end{array} \rightarrow\right| \begin{aligned} & 137 \mathrm{a}+23 \mathrm{~b}=18,3 \\ & \mathrm{a}+0,5 \mathrm{~b}=0,2\end{aligned} \rightarrow\left|\begin{array}{l}\mathrm{a}=0,1 \\ \mathrm{~b}=0,2\end{array} \rightarrow \downarrow\right| \begin{aligned} & \mathrm{BaSO}_{4}{ }^{0,4} \\ & \mathrm{Cu}(\mathrm{OH})_{2}{ }^{0,2}\end{aligned} \rightarrow \mathrm{m}=42,9 \rightarrow \mathrm{B}$
Câu 7: Ở trạng thải cơ bản, nguyên tử của nguyên tố nào sau đãy có 3 electron thuộc lớp ngoài củng:
A. ${ }_{7}^{14} \mathrm{~N}$
B. ${ }_{6}^{12} \mathrm{C}$
C. ${ }_{13}^{27} \mathrm{Al}$
D. ${ }_{11}^{23} \mathrm{Na}$
Câu 8: Hòa tan hoàn toàn một lượng hỗn hợp gổm $\mathrm{AI}, \mathrm{MgCO}_{3}, \mathrm{Fe}_{3} \mathrm{O}_{4}$ vào dung dịch $\mathrm{H}_{2} \mathrm{SO}_{4}$ loãng, thu được dung dịch $\mathrm{X}$. Cho dung dịch $\mathrm{Ba}(\mathrm{OH})_{2}$ tới dư vào dung dịch $\mathrm{X}$, sau khi các phản ứng xảy ra hoản toàn thu được kết tủa $\mathrm{Y}$. Nung $\mathrm{Y}$ trong không khí đến khối lượng không đổi thu được hỗn hợp rắn $\mathrm{Z}$ gồm:
A. $\mathrm{MgO}$ và $\mathrm{Fe}_{2} \mathrm{O}_{3}$
B. $\mathrm{BaSO}_{4}, \mathrm{MgO}_{\text {và } \mathrm{FeO}}^{\mathrm{Fe}}$
C. $\mathrm{BaSO}_{4}, \mathrm{MgO}_{\mathrm{a}}$ va $\mathrm{Fe}_{2} \mathrm{O}_{3}$
D. $\mathrm{BaSO}_{4}, \mathrm{MgO}, \mathrm{Al}_{2} \mathrm{O}_{3}$ và $\mathrm{Fe}_{2} \mathrm{O}_{3}$
Biết: $\mathrm{X}, \mathrm{Y}, \mathrm{Z}$ là các hợp chất khác nhau, mỗi mũi tên ứng với một phương trình hóa học. Các chất $\mathrm{E}, \mathrm{F}$ thỏa mãn sơ đồ trên lằn lượt là:
[Đỗ Kiên – 0948206996] – Hà Nội [ĐÈ THI HSG BĂC GIANG 2023]
A. $\mathrm{CO}_{2}, \mathrm{Na}_{2} \mathrm{CO}_{3}$
B. $\mathrm{H}_{2} \mathrm{O}, \mathrm{NaOH}$
C. $\mathrm{H}_{2} \mathrm{O}, \mathrm{CO}_{2}$
D. $\mathrm{CO}_{2}, \mathrm{H}_{2} \mathrm{O}$
Hướng dẫn
$\mathrm{CaO}+\mathrm{H}_{2} \mathrm{O} \rightarrow \mathrm{Ca}(\mathrm{OH})_{2}(\mathrm{X}) \quad \mathrm{Ca}(\mathrm{OH})_{2}+2 \mathrm{CO}_{2(\mathrm{du})} \rightarrow \mathrm{Ca}\left(\mathrm{HCO}_{3}\right)_{2}(\mathrm{Y})$
$\mathrm{CaO}+\mathrm{CO}_{2} \rightarrow \mathrm{CaCO}_{3}(\mathrm{Z}) \quad \mathrm{CaCO}_{3}+\mathrm{CO}_{2}+\mathrm{H}_{2} \mathrm{O} \rightarrow \mathrm{Ca}\left(\mathrm{HCO}_{3}\right)_{2}$
Câu 10: Hòa tan hoàn toàn 19,2 gam hỗn hợp $\mathrm{X}$ gồm $\mathrm{Fe}, \mathrm{FeO}, \mathrm{Fe}_{2} \mathrm{O}_{3}$ và $\mathrm{Fe}_{3} \mathrm{O}_{4}$ trong $400 \mathrm{ml}$ dung dịch $\mathrm{HNO}_{3}$ $3 \mathrm{M}$ dư, đun nóng, thu được dung dịch $\mathrm{Y}$ và $\mathrm{V}$ lít khí NO (sản phẩm khử duy nhất, ở đktc). Cho $350 \mathrm{ml}$ dung dịch $\mathrm{NaOH} 2 \mathrm{M}$ vào dung dịch $\mathrm{Y}$, sau khi các phản ứng xảy ra hoàn toàn, thu được 21,4 gam kết tủa. Giá trị $\mathrm{V}$ :
A. 3,36
B. 4,48
C. 5,04
D. 5,60
Hướng dẫn
Câu 11: Cho $\mathrm{m}$ gam hỗn hợp $\mathrm{X}$ gồm $\mathrm{Cu}, \mathrm{Fe}_{2} \mathrm{O}_{3}$ vào dung dịch $\mathrm{HCl}$ dư, thu được dung dịch $\mathrm{Y}$ và $0,5 \mathrm{~m}$ gam rắn không tan. Cho Y tác dụng với dung dịch $\mathrm{NaOH}$ dư thu được kết tủa Z. Nung Z trong không khí đến khối lượng không đổi thu được 24 gam hỗn hợp oxit. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m là:
A. 44,8
B. 48,0
C. 24,0
D. 32,6
Hướng dẫn
Câu 12: Nguyên tố R thuộc chu kì 3 , nhóm VIIA của bảng tuần hoàn các nguyên tố hóa học. Công thức oxit cao nhất của $\mathrm{R}$ là:
A. $\mathrm{R}_{2} \mathrm{O}_{3}$
B. $\mathrm{RO}_{3}$
C. $\mathrm{R}_{2} \mathrm{O}$
D. $\mathrm{R}_{2} \mathrm{O}_{7}$
Câu 13: Nghiền nhỏ 1 gam $\mathrm{CH}_{3} \mathrm{COONa}$ cùng với 2 gam vôi tôi xút $(\mathrm{CaO}, \mathrm{NaOH})$ rồi cho vào đáy ống nghiệm. Đun nóng đều ống nghiệm sau đó đun tập trung phần có chứa hỗn hợp phản ứng. Hidrocacbon sinh ra là:
A. Etan
B. Axetilen
C. Etilen
D. Metan
Câu 14 : Hỗn hợp $\mathrm{X}$ gồm $\mathrm{MgO}, \mathrm{Fe}_{2} \mathrm{O}_{3}, \mathrm{Fe}_{3} \mathrm{O}_{4}, \mathrm{CuO}$ trong đó oxi chiếm 27,78\% khối lượng. Cho $\mathrm{m}$ gam $\mathrm{X}$ phản ứng hết với dung dịch $\mathrm{HCl}$ vừa đủ, thu được dung dịch $\mathrm{Y}$ chứa 84,45 gam muối. Sục khí $\mathrm{Cl}_{2}$ dư vào $\mathrm{Y}$, thu được dung dịch $\mathrm{Z}$. Cho $\mathrm{Z}$ tác dụng với dung dịch $\mathrm{NaOH}$ dư, thu được 58,4 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Biết các phản ứng xảy ra hoàn toàn. Phần trăm khối lượng của $\mathrm{Fe}_{3} \mathrm{O}_{4}$ trong $\mathrm{X}$ gần nhất với giá trị sau :
A. $53,7 \%$
B. $61,8 \%$
C. $46,3 \%$
D. $53,3 \%$
Hướng dẫn
Câu 15 : Nung nóng $0,1 \mathrm{~mol} \mathrm{C}_{4} \mathrm{H}_{10}$ có xúc tác thích hợp, thu được hỗn hợp khí gồm $\mathrm{H}_{2}, \mathrm{CH}_{4}, \mathrm{C}_{2} \mathrm{H}_{4}, \mathrm{C}_{2} \mathrm{H}_{6}, \mathrm{C}_{3} \mathrm{H}_{6}$, $\mathrm{C}_{4} \mathrm{H}_{8}$ và $\mathrm{C}_{4} \mathrm{H}_{10}$. Dẫn $\mathrm{X}$ qua bình đựng dung dịch $\mathrm{Br}_{2}$ dư, sau khi phản ứng xảy ra hoàn toàn thấy khối lượng bình tăng $\mathrm{m}$ gam và có hỗn hợp khí $\mathrm{Y}$ thoát ra. Đốt cháy hoàn toàn $\mathrm{Y}$ cần vừa đủ 6,832 lít khí $\mathrm{O}_{2}$ (đktc). Giá trị $\mathrm{m}$ là :
A. 3,22
B. 2,80
C. 3,72
D. 4,20
Hướng dẫn
$\left|\begin{array}{l}\mathrm{C}_{4} \mathrm{H}_{10}{ }^{0,1} \rightarrow \mathrm{O}_{2}^{0,65} \\ \mathrm{Y} \rightarrow \mathrm{O}_{2}^{0,305}\end{array} \mathrm{O}_{2 \text { (anken) }}^{0,345} \rightarrow\right| \begin{aligned} & \mathrm{n}_{\mathrm{O}_{2}}=1,5 \mathrm{n}_{\mathrm{CO}_{2}} \\ & \mathrm{CO}_{2}^{0,23} \rightarrow \mathrm{H}_{2} \mathrm{O}^{0,23}\end{aligned} \rightarrow \mid \begin{aligned} & \text { Anken } \\ & \mathrm{m}=3,22,22 \mathrm{~g}\end{aligned}$
Câu 16 : Nung 40,8 gam hỗn hợp $\mathrm{X}$ gồm $\mathrm{Fe}$ và $\mathrm{Mg}$ có tỉ lệ mol tương ứng là $2: 1$ trong không khí một thời gian, thu được $\mathrm{m}$ gam hỗn hợp $\mathrm{Y}$ gồm kim loại và các oxit của chúng. Hòa tan hết lượng $\mathrm{Y}$ trong dung dịch $\mathrm{HNO}_{3}$ loãng dư, thu được 0,1 mol khí $\mathrm{NO}$ (duy nhất) và dung dịch $\mathrm{Z}$ chứa 190,6 gam muối. Giá trị của m là:
A. 148,0
B. 64,0
C. 68,0
D. 56,8
Hướng dẫn
Câu 17: Hỗn hợp $\mathrm{X}$ gồm $\mathrm{CH}_{4}, \mathrm{C}_{2} \mathrm{H}_{2}, \mathrm{C}_{2} \mathrm{H}_{6}$ và $\mathrm{C}_{2} \mathrm{H}_{4}$ có tỉ khối so với $\mathrm{H}_{2}$ là 12,55. Đốt cháy hoàn toàn a mol $\mathrm{X}$, sau đó dẫn toàn bộ sản phẩm cháy vào bình đựng dung dịch $\mathrm{Ca}(\mathrm{OH})_{2}$ dư, thu được 35 gam kết tủa trắng và thấy khối lượng bình tăng thêm 22,78 gam. Mặt khác, cho 1,004 gam $\mathrm{X}$ tác dụng với lượng dư dung dịch $\mathrm{Br}_{2}$, thấy lượng $\mathrm{Br}_{2}$ phản ứng tối đa là $\mathrm{x}$ mol. Giá trị của $\mathrm{x}$ là:
A. 0,016
B. 0,014
C. 0,030
D. 0,028
[Đỗ Kiên – 0948206996] – Hà Nội Hướng dẫn
$$
\left|\begin{array}{l}
\mathrm{CO}_{2}{ }^{0,35} \\
\mathrm{H}_{2} \mathrm{O}^{0,41}
\end{array} \rightarrow\right| \begin{aligned}
& \mathrm{CH}_{4}{ }^{\mathrm{b}} \\
& \mathrm{C}_{2} \mathrm{H}_{4}{ }^{\mathrm{c}} \\
& \mathrm{C}_{2} \mathrm{H}_{2}{ }^{\mathrm{d}}
\end{aligned} \rightarrow\left|\begin{array}{l}
\mathrm{b}+2 \mathrm{c}+2 \mathrm{~d}=0,35 \\
2 \mathrm{~b}+2 \mathrm{c}+\mathrm{d}=0,41 \\
16 \mathrm{~b}+28 \mathrm{c}+26 \mathrm{~d}=25,1(\mathrm{~b}+\mathrm{c}+\mathrm{d}) \\
(16 \mathrm{~b}+28 \mathrm{c}+26 \mathrm{~d}) \mathrm{k}=1,004
\end{array} \rightarrow\right| \begin{aligned}
& \mathrm{a}=0,05 \\
& \mathrm{~b}=0,16 \\
& \mathrm{c}=-0,01 \\
& \mathrm{k}=0,2
\end{aligned} \rightarrow \mathrm{x}=0,028 \rightarrow \mathrm{D}
$$
Câu 18: Hỗn hợp $\mathrm{X}$ gồm $\mathrm{C}_{2} \mathrm{H}_{4}$ và $\mathrm{H}_{2}$ có tỉ khối so với He bằng 3,75. Cho $\mathrm{X}$ bào bình có xúc tác $\mathrm{Ni}$, đun nóng, sau một thời gian phản ứng, thu được hỗn hợp $\mathrm{Y}$ có tỉ khối so với He bằng 6 . Hiệu suất phản ứng là:
A. $75 \%$
B. $50 \%$
C. $90 \%$
D. $60 \%$
Hướng dẫn
Câu 19: Hòa tan hết 7,52 gam hỗn hợp $\mathrm{X}$ gồm $\mathrm{M}_{2} \mathrm{CO}_{3}$ và $\mathrm{MHCO}_{3}$ vào dung dịch $\mathrm{HCl}$ dư, toàn bộ khí $\mathrm{CO}_{2}$ thoát ra được hấp thụ hết bởi lượng tối thiểu dung dịch chứa $0,06 \mathrm{~mol} \mathrm{NaOH}$ (bỏ qua sự tan của $\mathrm{CO}_{2}$ trong nước).
Cho $\mathrm{X}$ tác dụng với dung dịch $\mathrm{BaCl}_{2}$ dư, thu được khối lượng kết tủa là:
A. 11,82 gam
B. 39,40 gam
C. 59,10 gam
D. 7,88 gam
Hướng dẫn
$\left|\begin{array}{l}\mathrm{M}_{2} \mathrm{CO}_{3}{ }^{\mathrm{a}} \\ \mathrm{MHCO}_{3}{ }^{\mathrm{b}}\end{array} \rightarrow\right| \begin{aligned} & (2 \mathrm{M}+60) \mathrm{a}+(\mathrm{M}+61) \mathrm{b}=7,52 \\ & \mathrm{n}_{\mathrm{CO}_{2}}=\mathrm{a}+\mathrm{b}=0,06\end{aligned} \rightarrow \mid \begin{aligned} & \mathrm{M}=39 \rightarrow \mathrm{K} \\ & \mathrm{a}=0,04 \mathrm{l} b=0,02\end{aligned} \rightarrow \mathrm{BaCO}_{3}^{7,88 \mathrm{~g}} \rightarrow \mathrm{D}$
Câu 20: Cho các hidrocacbon sau: axetilen, metan, etilen, vinyl axetilen. Nhận xét nào sau đây là đúng:
A. Có hai hidrocacbon làm mất màu dung dịch $\mathrm{Br}_{2}$
B. Có một hidrocacbon pứ với $\mathrm{AgNO}_{3} / \mathrm{NH}_{3}$ tạo kết tủa
D. Có ba hidrocacbon có \% khối lượng $\mathrm{C}$ bằng $75 \%$
PHẦN TƯ’ LUẬN (14,0 điểm)
Câu 1: (3,0 điểm)
1. Cho sơ đồ phản ứng: $\mathrm{H}_{3} \mathrm{PO}_{4} \stackrel{+\mathrm{KOH}}{\longrightarrow} \mathrm{X} \stackrel{+\mathrm{H}_{3} \mathrm{PO}_{4}}{\longrightarrow} \mathrm{Y} \stackrel{+\mathrm{KOH}}{\longrightarrow} \mathrm{Z}$. Biết $\mathrm{X}, \mathrm{Y}, \mathrm{Z}$ là các hợp chất khác nhau của photpho. Xác định các chất $X, Y, Z$ và viết phương trình hóa học của các phản ứng theo sơ đồ đã cho.
2. Dung dịch $\mathrm{E}$ chứa $0,3 \mathrm{~mol} \mathrm{Ca}^{2+} ; \mathrm{x} \mathrm{mol} \mathrm{K} \mathrm{K}^{+} ; 0,54 \mathrm{~mol} \mathrm{Cl}^{-}$và y mol $\mathrm{HCO}_{3}{ }^{-}$. Cô cạn dung dịch $\mathrm{E}$, rồi lấy chất rắn đem nung đến khối lượng không đổi thu được 38,7 gam chất rắn. Tính giá trị của $\mathrm{x}$ và $\mathrm{y}$.
Hướng dẫn
1. $\mathrm{H}_{3} \mathrm{PO}_{4}+2 \mathrm{KOH} \rightarrow \mathrm{K}_{2} \mathrm{HPO}_{4}(\mathrm{X})+2 \mathrm{H}_{2} \mathrm{O} \quad \mathrm{K}_{2} \mathrm{HPO}_{4}+\mathrm{H}_{3} \mathrm{PO}_{4} \rightarrow 2 \mathrm{KH}_{2} \mathrm{PO}_{4}(\mathrm{Y})$
$\mathrm{KH}_{2} \mathrm{PO}_{4}+2 \mathrm{KOH} \rightarrow \mathrm{K}_{3} \mathrm{PO}_{4}(\mathrm{Z})+2 \mathrm{H}_{2} \mathrm{O}$
2. $\left|\begin{array}{l}\mathrm{Ca}^{2+(0,3)} \mid \mathrm{K}^{+(x)} \\ \mathrm{Cl}^{-(0,54)} \mid \mathrm{HCO}_{3}^{-(y)}\end{array} \rightarrow \mathrm{Rắ}^{\prime}\right| \begin{aligned} & \mathrm{Ca}^{2+} \mid \mathrm{K}^{+} \\ & \mathrm{Cl}^{-} \mid \mathrm{O}^{2-(0,5 y)}\end{aligned} \rightarrow\left|\begin{array}{l}\text { ВTDT } \\ 39 \mathrm{x}+8 \mathrm{x}+31,17=38,6=\mathrm{y}+0,54\end{array} \rightarrow\right| \begin{aligned} & \mathrm{x}=0,15 \\ & y=0,21\end{aligned}$
Câu 2: (3,0 điểm)
1. Cho hỗn hợp chất rắn gồm $\mathrm{Cu}, \mathrm{CuO}, \mathrm{Al}_{2} \mathrm{O}_{3}, \mathrm{Fe}_{2} \mathrm{O}_{3}$ vào dung dịch $\mathrm{H}_{2} \mathrm{SO}_{4}$ loãng dư, thu được dung dịch $\mathrm{X}$ và chất rắn $\mathrm{Y}$. Cho từ từ đến dư dung dịch $\mathrm{NaOH}$ vào $\mathrm{X}$, thu được dung dịch $\mathrm{Z}$ và kết tủa $\mathrm{T}$. Nung $\mathrm{T}$ trong không khí đến khối lượng không đổi, thu được chất rắn $\mathrm{E}$. Dẫn khí $\mathrm{CO}$ dư đi qua $\mathrm{E}$ nung nóng, thu được chất rắn $\mathrm{F}$. Sục khí $\mathrm{CO}_{2}$ dư vào $\mathrm{Z}$, thu được kết tủa $\mathrm{G}$. Biết các phản ứng xảy ra hoàn toàn. Xác định thành phần các chất trong $\mathrm{X}, \mathrm{Y}, \mathrm{Z}, \mathrm{T}, \mathrm{E}, \mathrm{F}, \mathrm{G}$ và viết các phương trình hóa học của các phản ứng xảy ra.
Hướng dẫn
$\mathrm{CuO}+\mathrm{H}_{2} \mathrm{SO}_{4} \rightarrow \mathrm{CuSO}_{4}+\mathrm{H}_{2} \mathrm{O} \quad \mathrm{Al}_{2} \mathrm{O}_{3}+3 \mathrm{H}_{2} \mathrm{SO}_{4} \rightarrow \mathrm{Al}_{2}\left(\mathrm{SO}_{4}\right)_{3}+3 \mathrm{H}_{2} \mathrm{O} \quad \mathrm{Fe}_{2} \mathrm{O}_{3}+3 \mathrm{H}_{2} \mathrm{SO}_{4} \rightarrow \mathrm{Fe}_{2}\left(\mathrm{SO}_{4}\right)_{3}+3 \mathrm{H}_{2} \mathrm{O}$
$\mathrm{Cu}+\mathrm{Fe}_{2}\left(\mathrm{SO}_{4}\right)_{3} \rightarrow \mathrm{CuSO}_{4}+2 \mathrm{FeSO}_{4} \quad \mathrm{Al}_{2}\left(\mathrm{SO}_{4}\right)_{3}+8 \mathrm{NaOH} \rightarrow 3 \mathrm{Na}_{2} \mathrm{SO}_{4}+2 \mathrm{NaAlO}_{2}+4 \mathrm{H}_{2} \mathrm{O}$
$\mathrm{CuSO}_{4}+2 \mathrm{NaOH} \rightarrow \mathrm{Cu}(\mathrm{OH})_{2}+\mathrm{Na}_{2} \mathrm{SO}_{4} \quad \mathrm{FeSO}_{4}+2 \mathrm{NaOH} \rightarrow \mathrm{Na}_{2} \mathrm{SO}_{4}+\mathrm{Fe}(\mathrm{OH})_{2} \quad \mathrm{Cu}(\mathrm{OH})_{2} \rightarrow \mathrm{CuO}+\mathrm{H}_{2} \mathrm{O}$
$2 \mathrm{Fe}(\mathrm{OH})_{2}+1 / 2 \mathrm{O}_{2} \rightarrow \mathrm{Fe}_{2} \mathrm{O}_{3}+2 \mathrm{H}_{2} \mathrm{O} \quad \mathrm{CO}_{2}+\mathrm{NaAlO}_{2}+\mathrm{H}_{2} \mathrm{O} \rightarrow \mathrm{NaHCO}_{3}+\mathrm{Al}(\mathrm{OH})_{3}$
2. Dung dịch $\mathrm{X}$ gồm $0,4 \mathrm{~mol} \mathrm{HCl}$ và $0,05 \mathrm{~mol} \mathrm{Cu}\left(\mathrm{NO}_{3}\right)_{2}$. Cho $\mathrm{m}$ gam bột $\mathrm{Fe}$ vào dung dịch $\mathrm{X}$ khuấy đều cho đến khi phản ứng kết thúc, thu được $\mathrm{V}$ lít khí $\mathrm{NO}$ (sản phẩm khử duy nhất của $\mathrm{NO}_{3}{ }^{\circ}$, đktc) và chất rắn $\mathrm{Y}$ gồm hai kim loại có khối lượng $0,8 \mathrm{~m}$ gam. Viết phương trình phản ứng xảy ra và tính giá trị $\mathrm{m}, \mathrm{V}$.
Hướng dẫn
Rắn gồm $\mathrm{Fe}$ dư, $\mathrm{Cu}$ và $4 \mathrm{H}^{+}+\mathrm{NO}_{3}{ }^{-}+3 \mathrm{e} \rightarrow \mathrm{NO}+2 \mathrm{H}_{2} \mathrm{O}$ vậy sau pứ $\mathrm{H}^{+}$và $\mathrm{NO}_{3}{ }^{-}$đều hết $\mathrm{nNO}=0,1 \rightarrow \mathrm{V}=2,24$
Câu 3: (4,0 điểm)
1. Một hợp chất ion $\mathrm{A}$ cấu tạo từ hai ion $\mathrm{M}^{2+}$ và $\mathrm{X}^{-}$. Các ion được tạo ra từ các nguyên tử tương ứng. Trong phân tử $\mathrm{A}$ có tồng số hạt proton, notron và electron là 186 hạt, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 54 hạt. Số khối của $\mathrm{M}^{2+}$ lớn hơn số khối của $\mathrm{X}^{-}$là 21 . Tổng số hạt proton, notron và electron trong ion $\mathrm{M}^{2+}$ nhiều hơn trong ion $\mathrm{X}^{-}$là 27 hạt. Viết cấu hình electron của nguyên tử $\mathrm{M}, \mathrm{X}$ và của ion $\mathrm{M}^{2+}, \mathrm{X}^{-}$.
Hướng dẫn
2. Hỗn hợp $\mathrm{X}$ gồm $\mathrm{Mg}$ và kim loại $\mathrm{R}$ có hóa trị không đổi. Để hòa tan hoàn toàn 21,56 gam $\mathrm{X}$ cần vừa đủ $\mathrm{V}$ lít dung dịch $\mathrm{HNO}_{3} 0,75 \mathrm{M}$ thu được 0,784 lít hỗn hợp khí $\mathrm{Y}$ gồm $\mathrm{N}_{2}, \mathrm{~N}_{2} \mathrm{O}$ (đktc) và dung dịch $\mathrm{Z}$. Chia $\mathrm{Z}$ thành hai phần bằng nhau. Đem cô cạn phần một thu được 39,41 gam muối khan. Phần hai cho tác dụng với dung dịch $\mathrm{KOH}$ dư, thu được 4,06 gam kết tủa. Biết tỉ khối của $\mathrm{Y}$ so với $\mathrm{H}_{2}$ bằng 17,2 và trong quá trình cô cạn không xảy ra phản ứng hóa học. Xác định kim loại $\mathrm{R}$ và tính giá trị của $\mathrm{V}$.
Hướng dẫn
Nếu $\mathrm{R}(\mathrm{OH})_{\mathrm{n}}$ không tan trong $\mathrm{KOH}$ dư.
$\operatorname{Mol} \mid \begin{aligned} & \mathrm{Mg}^{\mathrm{a}} \\ & \mathrm{R}^{\mathrm{b}} \\ & \mathrm{NH}_{4}{ }^{+(\mathrm{c})}\end{aligned} \rightarrow$ Muối $\left|\begin{array}{l}\mathrm{Mg}\left(\mathrm{NO}_{3}\right)_{2}{ }^{\mathrm{a}} \\ \mathrm{R}\left(\mathrm{NO}_{3}\right)_{\mathrm{n}}{ }^{\mathrm{b}} \\ \mathrm{NH}_{4} \mathrm{NO}_{3}{ }^{\mathrm{c}}\end{array} \rightarrow\right| \begin{aligned} & 24 \mathrm{a}+\mathrm{Rb}=21,56 \\ & \stackrel{\mathrm{BT} . \mathrm{e}}{\longrightarrow} 2 \mathrm{a}+\mathrm{nb}=8 \mathrm{c}+0,322 \\ & 148 \mathrm{a}+(\mathrm{R}+62 \mathrm{n}) \mathrm{b}+80 \mathrm{c}=78,82 \\ & 58 \mathrm{a}+(\mathrm{R}+17 \mathrm{n}) \mathrm{b}=8,12\end{aligned} \stackrel{\mathrm{n}=1,2,3}{\longrightarrow} \mathrm{vôn}^{\circ}$ nên $\mathrm{R}(\mathrm{OH})_{\mathrm{n}}$ tan trong KOH
$12 \mathrm{HNO}_{3}+10 \mathrm{e} \rightarrow 10 \mathrm{NO}_{3}{ }^{-}+\mathrm{N}_{2}+6 \mathrm{H}_{2} \mathrm{O} \quad 10 \mathrm{HNO}_{3}+8 \mathrm{e} \rightarrow 8 \mathrm{NO}_{3}{ }^{-}+\mathrm{N}_{2} \mathrm{O}+5 \mathrm{H}_{2} \mathrm{O}$
$10 \mathrm{HNO}_{3}+8 \mathrm{e} \rightarrow 8 \mathrm{NO}_{3}^{-}+\mathrm{NH}_{4} \mathrm{NO}_{3}+3 \mathrm{H}_{2} \mathrm{O} \quad$ Vậy: $\mathrm{nHNO}_{3}=12 \mathrm{nN}_{2}+10 \mathrm{n}\left(\mathrm{N}_{2} \mathrm{O}+\mathrm{NH}_{4} \mathrm{NO}_{3}\right) \rightarrow \mathrm{V}=1,386(1)$
Câu 4: (4,0 điểm)
1. Hỗn hợp $\mathrm{A}$ gồm hai chất hữu cơ $\mathrm{X}\left(\mathrm{C}_{\mathrm{n}} \mathrm{H}_{2 \mathrm{n}+3} \mathrm{~N}\right), \mathrm{Y}\left(\mathrm{C}_{\mathrm{n}} \mathrm{H}_{2 \mathrm{n}+4} \mathrm{~N}_{2}\right.$, với $\left.\mathrm{n} \geq 2\right)$ và hai anken đồng đẳng kế tiếp. Đốt cháy hoàn toàn $0,15 \mathrm{~mol} \mathrm{~A}$ bằng khí $\mathrm{O}_{2}$ thu được $0,06 \mathrm{~mol} \mathrm{~N}_{2} ; 0,42 \mathrm{~mol} \mathrm{CO}_{2}$ và $0,57 \mathrm{~mol} \mathrm{H}_{2} \mathrm{O}$. Xác định công thức phân tử của các chất trong $\mathrm{A}$ và viết công thức cấu tạo của $\mathrm{X}$.
Hướng dẫn
Cách 1: Để cụ thể, ta qui về các chất đơn giản nhất thoải mãn tính chất các chất đề bài cho.
2. Cho ankan $\mathrm{X}$ và hai ankin $\mathrm{Y}, \mathrm{Z}$ đều có số nguyên tử cacbon nhỏ hơn $5\left(\mathrm{M}_{\mathrm{Y}}<\mathrm{M}_{\mathrm{Z}}\right)$. Đốt cháy hoàn toàn hỗn hợp $\mathrm{A}$ gồm $\mathrm{Y}$ và $\mathrm{Z}$, thu được 6,048 lít khí $\mathrm{CO}_{2}$ (đktc) và 3,24 gam $\mathrm{H}_{2} \mathrm{O}$. Thêm một lượng $\mathrm{X}$ vào $\mathrm{A}$ được hỗn hợp B. Đốt cháy hoàn toàn $\mathrm{V}$ lít $\mathrm{B}$, thu được $3 \mathrm{~V}$ lít $\mathrm{CO}_{2}$ (trong cùng điều kiện về nhiệt độ và áp suất). Xác định công thức cấu tạo của $\mathrm{X}, \mathrm{Y}, \mathrm{Z}$ và tính $\%$ thể tích của $\mathrm{X}$ trong $\mathrm{B}$. Biết khi cho 2,24 lít khí $\mathrm{B}$ (đktc) tác dụng với lượng dư dung dịch $\mathrm{AgNO}_{3}$ trong $\mathrm{NH}_{3}$ thì thu được 9,624 gam kết tủa.
Hướng dẫn
Công thức cấu tạo của $\mathrm{X}: \mathrm{CH}_{3} \mathrm{CH}_{2} \mathrm{CH}_{3} ; \mathrm{Y}: \mathrm{CH} \equiv \mathrm{CH} ; \mathrm{Z}$ : $\mathrm{CH} \equiv \mathrm{C}-\mathrm{CH}_{2} \mathrm{CH}_{3}$.