File word Đề thi thử vào 10 chuyên Ngôi Sao Hà Nội – Năm học 2023
File word Đề thi thử vào 10 chuyên Ngôi Sao Hà Nội – Năm học 2023
Câu 1: (4,0 điểm)
1. Cho sơ đồ phản ứng sau:
Xác định các chất $\mathrm{A}, \mathrm{B}, \mathrm{C}, \mathrm{D}, \mathrm{E}, \mathrm{F}, \mathrm{G}$ (có thể là chất vô cơ hoặc hữu cơ) và viết các phương trình hóa học hoàn thành sơ đồ phản ứng trên; biết $\mathrm{A}$ là hợp chất trong đó nhôm chiếm $75 \%$ về khối lượng; $\mathrm{C}$ và $\mathrm{D}$ là các chất có khả năng làm mất màu dung dịch brom; $\mathrm{G}$ là chất rắn không tan trong nước.
2. Có bốn dung dịch không màu $\mathrm{X}, \mathrm{Y}, \mathrm{Z}, \mathrm{T}$; trong mỗi dung dịch có chứa một chất tan là một hợp chất của natri hoặc bari. Người ta lần lượt tiến hành các thí nghiệm như sau:
– Lần lượt đổ dung dịch $X$ vào các dung dịch $\mathrm{Y}$ và $\mathrm{Z}$ đều không thấy có hiện tượng gì xảy ra.
– Đổ dung dịch $Y$ vào dung dịch $\mathrm{Z}$, không có hiện tượng gì. Tiếp tục đổ dung dịch $\mathrm{X}$ vào dung dịch sau phản ứng thì thấy xuất hiện kết tủa trắng.
– Đổ dung dịch $\mathrm{Z}$ vào dung dịch $\mathrm{T}$ thấy thoát ra một khí không màu, không mùi. Tiếp tục đổ dung dịch $\mathrm{X}$ vào dung dịch sau phản ứng thì cũng thấy xuất hiện kết tủa trắng.
Hãy lập luận để xác định mỗi dung dịch $\mathrm{X}, \mathrm{Y}, \mathrm{Z}, \mathrm{T}$ có thể chứa chất tan nào? Câu 2: $(3,0$ điểm $)$
1. Cho $\mathrm{V}$ lít khí $\mathrm{CO}$ (đktc) đi qua ống sứ chứa $0,15 \mathrm{~mol} \mathrm{FeO}$ và $\mathrm{Fe}_2 \mathrm{O}_3$ (hỗn hợp $\mathrm{A}$ ) nung nóng. Sau một thời gian thu được hỗn hợp rắn $\mathrm{B}$ nặng 12 gam gồm bốn chất và khí $\mathrm{X}$ có tỉ khối so với $\mathrm{H}_2$ là 20,4 . Cho $\mathrm{X}$ vào dung dịch $\mathrm{Ca}(\mathrm{OH})_2$ dư thu được 20 gam kết tủa.
a. Tính $\mathrm{V}$ và $\%$ khối lượng mỗi chất trong $\mathrm{A}$
b. Hòa tan hết $\mathrm{B}$ vào dung dịch $\mathrm{H}_2 \mathrm{SO}_4$ đặc nóng thu được 37,12 gam muối và $\mathrm{V}$ ‘ lít khí $\mathrm{SO}_2$ (đktc). Tính $\mathrm{V}^{\prime}$.
2. Hòa tan hết 6,08 gam hỗn hợp gồm $\mathrm{Cu}$ và $\mathrm{Fe}$ bằng dung dịch $\mathrm{H}_2 \mathrm{SO}_4$ đặc thu được dung dịch $\mathrm{A}$ và 2,688 lít $\mathrm{SO}_2$ (đktc). Thêm từ từ 2,88 gam bột $\mathrm{Mg}$ vào dung dịch $\mathrm{A}$ đến khi phản ứng xảy ra hoàn toàn thu được 0,672 lít $\mathrm{SO}_2$ (đktc), dung dịch $\mathrm{B}$ và $\mathrm{m}$ gam chất rắn không tan $\mathrm{D}$. Xác định thành phần của $\mathrm{D}$ và tính $\mathrm{m}$.
Câu 3: (5,0 điểm)
1. Hòa tan hoàn toàn $\mathrm{m}$ gam hỗn hợp $\mathrm{X}$ gồm $\mathrm{Ba}, \mathrm{BaO}, \mathrm{Na}, \mathrm{Na}_2 \mathrm{O}, \mathrm{Al}$ và $\mathrm{Al}_2 \mathrm{O}_3$ vào nước thu được dung dịch $\mathrm{Y}$ và 12,32 lít khí (đktc). Cho từ từ dung dịch $\mathrm{H}_2 \mathrm{SO}_4 2 \mathrm{M}$ vào dung dịch $\mathrm{Y}$, mối quan hệ giữa khối lượng kết tủa thu được và thể tích $\mathrm{V} \mathrm{ml}$ của dung dịch $\mathrm{H}_2 \mathrm{SO}_4$ sử dụng được thể hiện trong đồ thị dưới đây:
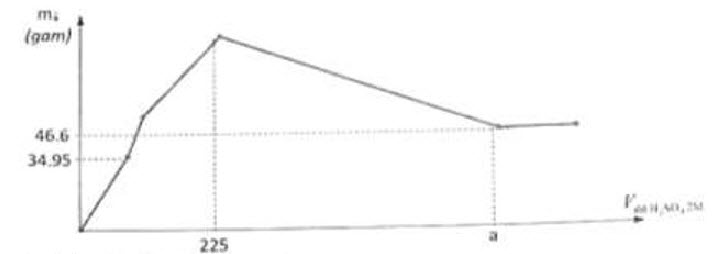
Xác định giá trị của a và tính $\mathrm{m}$.
2. Từ không khí, nước, than đá, quặng photphorit, quặng pirit sắt, hãy viết các phương trình phản ứng điều chế các loại phân bón hóa học: ure, supephotphat đơn, supephotphat kép, amophot $\left(\mathrm{NH}_4 \mathrm{H}_2 \mathrm{PO}_4\right)$.
Câu 4: (3,0 điểm )
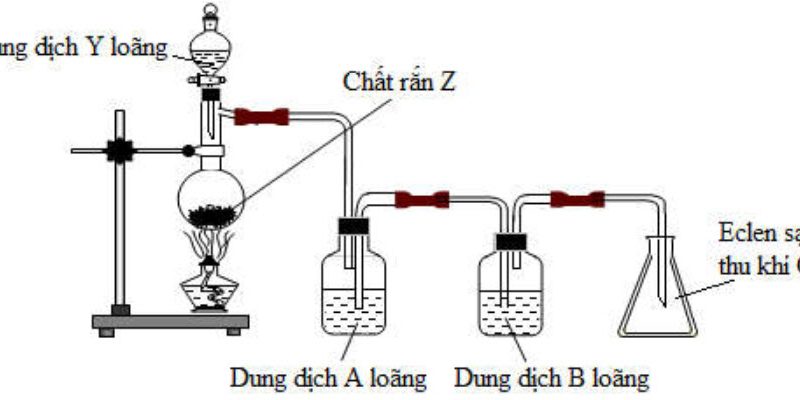
1. Cho sơ đồ bộ thí nghiệm như hình vẽ:
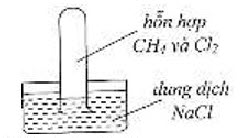
– Tại sao lại sử dụng dung dịch $\mathrm{NaCl}$ trong chậu thủy tinh.
– Đem bộ thí nghiệm này để ra ngoái ánh sáng. Nêu hiện tượng quan sát được và giải thích.
2. Cho các kim loại sau: đồng, nhôm, natri, bạc.
a. Chỉ ra hai kim loại dẫn điện tốt nhất
b. Tính thể tích 1 mol kim loại đồng biết khối lượng riêng $\mathrm{d}_{\mathrm{Cu}}=8,94 \mathrm{~g} / \mathrm{ml}$
c. Tại sao đồ vật bằng nhôm trong không khí
d. Nêu cách bảo quản natri trong phòng thí nghiệm
Câu 5: (5,0 điểm)
1. Hỗn hợp khí $\mathrm{A}$ gồm một ankan và hai ankin liên tiếp nhau có thể tích 5,6 lít (đktc). Đốt cháy hoàn toàn hỗn hợp $\mathrm{A}$ thu được 10,304 lít đktc) khí $\mathrm{CO}_2$ và 7,38 gam $\mathrm{H}_2 \mathrm{O}$.
a. Xác định công thức phân tử và tính \% thể tích mỗi chất trong hỗn hợp $\mathrm{A}$.
b. Trộn hỗn hợp $\mathrm{A}$ với $\mathrm{V}$ lít (đktc) khí $\mathrm{H}_2$ thu được hỗn hợp $\mathrm{B}$. Nung nóng hỗn hợp $\mathrm{B}$ với xúc tác Ni tới phản ứng xảy ra hoàn toàn thu được hỗn hợp $\mathrm{D}$. Dẫn hỗn hợp $\mathrm{X}$ vào bình dung dịch brom dư thấy khối lượng bình brom tăng lên 2,18 gam và thoát ra 4,032 lít (đktc) hỗn hợp khí $\mathrm{E}$ có tỉ khối so với $\mathrm{H}_2$ là $38: 3$. Tính giá trị của $\mathrm{V}$ và khối lượng oxi cần dùng để đốt cháy hoàn toàn hỗn hợp $\mathrm{D}$.
2. Hỗn hợp $\mathrm{X}$ gồm hai ancol $\mathrm{C}_{\mathrm{n}} \mathrm{H}_{2 \mathrm{n}+1} \mathrm{OH}$ và $\mathrm{C}_{\mathrm{n}} \mathrm{H}_{2 \mathrm{n}}(\mathrm{OH})_2$. Cho hỗn hợp $\mathrm{X}$ tác dụng với lượng dư kim loại Na thu được 4,48 lít khí (đktc). Mặt khác, để đốt cháy hoàn toàn hỗn hợp $\mathrm{X}$ cần dùng 23,52 lít (đktc) khí $\mathrm{O}_2$; toàn bộ sản phẩm cháy được hấp thụ vào bình đựng dung dịch nước vôi trong dư, thấy khối lượng bình tăng 51 gam. a. Xác định công thức của hai ancol trong $X$ và tính \% khôi lượng mỗi ancol trong $X$.
b. Trộn hỗn hợp X với 18 gam axit axetic được hỗn hợp Y. Đun hỗn hợp $\mathrm{Y}$ với $\mathrm{H}_2 \mathrm{SO}_4$ đặc để thực hiện phản ứng este hóa; sau một thời gian thu được hỗn hợp các chất hữu cơ $\mathrm{Z}$ có khối lượng 31,08 gam. Biết các chất có nhóm chức este trong $Z$ có số mol bằng nhau. Hãy tính \% mỗi ancol và \% axit axetic đã chuyển hóa thành este.