File Word đề thi HSG Hoá 9 Hà Nội – Năm học 2022 – 2023
Wchem9 đã Word hoá đề thi HSG Hoá 9 Hà Nội – Năm học 2022 – 2023 nay chia sẻ cùng các bạn
Hình ảnh đề thi HSG Hoá 9 Hà Nội – Năm học 2022 – 2023

Nội dung đề thi HSG Hoá 9 Hà Nội – Năm học 2022 – 2023
Câu I (4,0 điểm)
1. a) Vì sao muối NaHCO3 được dùng để chế thuốc đau dạ dày?
b) Làm thế nào để quá trình hòa tan chất rắn trong nước xảy ra nhanh hon? Giải thích.
c) Trước khi thi đấu. các vận động viên môn thể dục dụng cụ thường xoa lòng bàn tay vào chất bột màu trắng (MgCO3). Vì sao họ làm như vậy?
2. Từ oleum (H2SO4.3SO3), trình bày cách pha chế 2 lít dung dịch H2SO4 1M.
3. Hoàn thành các phương trình hóa học sau:
a) P2O5 + ………… -> Ca3(PO4)2 + ……
b) Cu(OH)2 + ………… -> Cu(NO3)2 + ……
c) SO2 + Br2 + H2O -> ……………. + …….
d) …….. + AgNO3 -> Zn(NO3)2 + ……….
e) KMNO4 + HClđặc -> … + … + … + …
f) Ca(HCO3)2 +…… -> NaHCO3 + …
Câu II (4,0 điểm)
1. Nêu hiện tượng, giải thích và viết phương trình hóa học xảy ra cho các thí nghiệm sau:
a) Cho dung dịch natri hiđroxit tới dư vào dung dịch sắt (II) clorua, sau đó để ngoài không khí.
b) Nhỏ 1 – 2 ml dung dịch axit sunfuric vào ống nghiệm dựng một ít bột đồng (II) oxit, lắc nhẹ.
c) Nhúng một sợi dây đồng đã được làm sạch vào dung dịch sắt (III) clorua.
d) Cho một mấu nhỏ canxi oxit vào ống nghiệm, nhỏ vài giọt nước vào canxi oxit. Tiếp tục cho thêm nước, dùng đủa thủy tinh trộn đều. Để yên ống nghiệm một thời gian rồi nhỏ thêm vài giọt dung dịch
2. Cho 5 dung dịch đựng trong 5 lọ mất nhãn: Ba(NO3)2, K2CO3, MgCl2, Na2SO4, K3PO4 được kí hiệu bằng các chữ cái A, B, C, D, E (không theo trình tự trên). Kết quả của một số thí nghiệm tìm hiểu về những chất này được ghi trong bảng sau:
| Mẫu thử | Thí nghiệm | Hiện tượng |
| A | Tác dụng với dung dịch chứa chất c hoặc D | Có kết tủa trẳng |
| B | Tác dụng với dung dịch chứa chất D | Có kểt tủa trắng |
| C | Tác dụng với dung dịch chứa chất A hoặc E | Có kết tủa trăng |
| D | Tác dụng với dung dịch chứa chất A hoặc B hoặc E | Có kết tủa trắng |
Biết rằng kết tủa sinh ra do dung dịch chứa chất A phản ứng với dung dịch chứa chất C bị phân hủy ở nhiệt độ cao tạo ra oxit kim loại. Xác định các chất A, B, C, D, E và viết phương trình hóa học minh họa.
3. Khi nung nóng, các muối ngậm nước sẽ giảm dần khối lượng do nước tách ra trước sau đó đến phản ứng nhiệt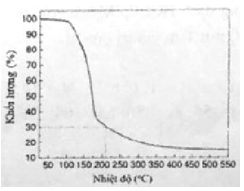 phân muối khan. Sự giảm khối lượng của muối Al(NO3)3.9H2O theo nhiệt độ được biểu diễn như giản đồ hình bên. Tại nhiệt độ 21O°C, phần chất rắn còn lại (chứa ba nguyên tố) có khối lượng bằng 30% khối lượng ban đầu. Tính thành phần phần trăm theo khối lượng của oxi có trong phần chất rắn tại 21 O°c.
phân muối khan. Sự giảm khối lượng của muối Al(NO3)3.9H2O theo nhiệt độ được biểu diễn như giản đồ hình bên. Tại nhiệt độ 21O°C, phần chất rắn còn lại (chứa ba nguyên tố) có khối lượng bằng 30% khối lượng ban đầu. Tính thành phần phần trăm theo khối lượng của oxi có trong phần chất rắn tại 21 O°c.
Câu III (4,0 điểm)
1. Hợp chất MX3 được sử dụng làm chất xúc tác trong tổng hợp hữu cơ. Tổng số hạt proton, nơtron, electron trong hợp chất MX3 là 196, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 60. Tồng số hạt trong hạt nhân cùa M nhỏ hơn tổng số hạt trong hạt nhân của X là 8. Tổng số hạt proton, nơtron, electron trong một nguyên tử X nhiều hơn trong một nguyên tử M là 12. Xác định công thức của MX3.
2. Hòa tan hoàn toàn m gam hỗn hợp gồm K, K2O, KOH và K2CO3 bằng dung dịch H2SO4 10% vừa đủ thu được 0.896 lít (đktc) hỗn hợp khí có tỉ khối đối với H2 bằng 11,5 và dung dịch Y chỉ chứa muối trung hòa có nồng độ 16,246%. Cô cạn Y thu được 10.44 gam chất rắn khan. Viết các phương trình hóa học xảy ra và tìm giả trị của m.
3. Hòa tan hoàn toàn a mol CuO bằng một lượng vừa đù dung dịch H2SO4 10%, đun nóng, thu được dung dịch X. Làm lạnh X đến 10°C thì có 1,472 gam tinh thể CuSO4.5H2O tách ra. Biết ở 10°C, cứ 100 gam H2O hòa tan được tối đa 17,4 gam CuSO4. Tìm giá trị của a.
Câu IV (4.0 điếm)
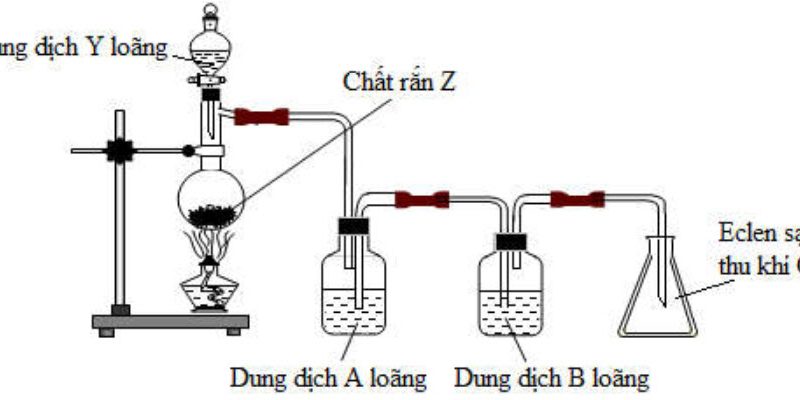
1. Hình vẽ bên mô tả thí nghiệm điều chế khí H2 trong phòng thí nghiệm, hãy cho biết:
a) Hóa chất cần dùng ở (1) và (2) là gì? Viết phương trình hóa học minh họa.
b) Khí H2 đã thu được bằng phương pháp gì? Phương pháp này dựa trên tính chất nào của H2?
2. Nung hỗn hợp X gồm KClO3 và KMnO4, thu được hỗn hợp chất rắn Y và O2. Trong Y có 1,49 gam KCl chiếm 17,028% theo khối lượng. Lượng O2 ở trên đốt cháy hết 0,24 gam cacbon, sau phản ứng thu được hỗn hợp khí T gồm CO2 và O2 dư (CO2 chiếm 40% thể tích). Biết KClO3 bị nhiệt phân hoàn toàn, còn KMnO4 chỉ bị nhiệt phân một phần. Tính hiệu suất của phản ứng nhiệt phân KMnO4.
3. Cho 10,332 gam hỗn hợp X gồm Fe, FeO, Fe2O3, chia X thành 3 phần bằng nhau. Dẫn khí H2 tới dư đi qua phần 1 nung nóng, thu được 2,604 gam Fe. Cho phần 2 vào dung dịch CuSO4 dư, sau phản ứng lọc bỏ dung dịch thu được 3,504 gam chất rắn. Hòa tan hết phần 3 trong dung dịch HCl thu được 0,1344 lít (đktc) khí H2 và dung dịch Y chỉ chứa 2 muối. Cho Y tác dụng với dung dịch AgNO3 dư, thu dược m gam chất rắn. Biết các phản ứng xảy ra hoàn toàn. Tìm giá trị của m.
Câu V (4.0 điểm)
1. Hấp thụ hết 3,08 gam khí CO2 bằng dung dịch chứa hỗn hợp X mol Ca(OH)2 và y mol NaOH thu dược 1 gam kết tủa và dung dịch chỉ chứa 4,98 gam muối. Tìm giá trị cùa X và Y.
2. Nung nóng m gam hỗn hợp X gồm Zn, AI và Cu trong O2 dư thu được 6,06 gam hỗn hợp Y chỉ gồm các oxit. Hòa tan hết Y bằng một lượng vừa đủ dung dịch gồm HCl 0,5M và H2SO4 0,25M, thu được dung dịch chỉ chứa 13,485 gam hỗn hợp muối trung hòa. Tìm giá trị của m.
3. Nung m gam hỗn hợp gồm KHCO3 và CaCO3 ở nhiệt độ cao đến khối lượng không đổi thu được chất rắn X. Cho X vào lượng nước dư, sau phản ứng thu được chất rắn Y và dung dịch Z. Chia Z thành hai phần bằng nhau. Cho dung dịch Ca(HCO3)2 tới dư vào phần 1, sau phản ứng thu dược 3 gam kết tủa. Cho từ từ dung dịch HCl 0,2M vào phần 2 đến khi không còn khí thoát ra thì thề tích dung dịch HCl đã dùng là 200 ml. Tìm giá trị của m.
Cho: H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; S = 32; Cl =35,5; K = 39; Ca = 40; Mn = 55; Fe = 56; Cu = 64; Zn = 65; Br = 80; Ag = 108; Ba = 137.
File Word đề thi HSG Hoá 9 Hà Nội – Năm học 2022 – 2023
Bạn hãy comment để lại mail mình share cho