Đề thi HSG Hoá 9 Tỉnh Phú Thọ – Năm học 2022 – 2023
Đề thi HSG Hoá 9 Tỉnh Phú Thọ – Năm học 2022 – 2023





ĐÊ CHÍNH THÚ’C
LOP 9 THCS NAM HỌC 2022-2023
MÔN: HÓA HỌC
Thời gian làm bài: 150 phút, không kể thời gian giao đề
(Dề thi có 05 trang)
Cho nguyên tử khối (đvC):
$\mathrm{H}=1 ; \mathrm{C}=12 ; \mathrm{N}=14 ; \mathrm{O}=16 ; \mathrm{F}=19 ; \mathrm{Na}=23 ; \mathrm{Mg}=24 ; \mathrm{Al}=27 ; \mathrm{P}=31 ; \mathrm{S}=32 ; \mathrm{Cl}=35,5$; $\mathrm{K}=39 ; \mathrm{Ca}=40 ; \mathrm{Mn}=55 ; \mathrm{Fe}=56 ; \mathrm{Cu}=64 ; \mathrm{Zn}=65 ; \mathrm{Si}=28 ; \mathrm{Ag}=108 ; \mathrm{Pb}=207 ; \mathrm{Ba}=137$. A. PHẤN TRÁC NGHIẸM KHÁCH QUAN: (10,0 diểm gồm 20 câu)
Câu 1: Cho các chất sau: $\mathrm{NaCl}, \mathrm{CaSO}_4, \mathrm{Ba}\left(\mathrm{HCO}_3\right)_2, \mathrm{Na}_2 \mathrm{CO}_3, \mathrm{Ca}_3\left(\mathrm{PO}_4\right)_2$. Số muối tan tốt trong nước ở nhiệt độ phòng lả
A. 2.
B. 5 .
C. 4 .
D. 3 .
Câu 2: Thí nghiệm nào dưới đây thu được kết tủa sau khi kết thúc các phản ứng hóa học?
A. Sục khi $\mathrm{SO}_2$ vào dung dịch $\mathrm{NaOH}$ dư.
B. Sục khi $\mathrm{CO}_2$ vào dung dịch $\mathrm{BaCl}_2$ dư.
C. Sục khi $\mathrm{CO}_2$ dư vào dung dịch $\mathrm{Ba}(\mathrm{OH})_2$.
D. Cho dung dịch $\mathrm{AlCl}_3$ dư vào dung dịch $\mathrm{NaOH}$.
Câu 3: Biết:
– Khí $\mathrm{X}$ rất độc, không cháy, hoà tan trong nước, nặng hơn không khí và có tính tầy màu.
– Khí Y rất độc, cháy trong không khi với ngọn lửa màu xanh sinh ra chất khí làm đục nước vôi trong.
– Khí Z không cháy, nặng hơn không khi, làm đục nước vôi trong.
$\mathrm{X}, \mathrm{Y}, \mathrm{Z}$ lần lượt là
A. $\mathrm{Cl}_2, \mathrm{CO}, \mathrm{CO}_2$.
B. $\mathrm{Cl}_2, \mathrm{SO}_2, \mathrm{CO}_2$.
C. $\mathrm{SO}_2, \mathrm{H}_2, \mathrm{CO}_2$.
D. $\mathrm{H}_2, \mathrm{CO}, \mathrm{SO}_2$.
(a) Do hoạt động của núi lừa.
(b) Do khí thải công nghiệp, khí thải sinh hoạt.
(c) Do khí thải từ các phương tiện giao thông.
(d) Do khi sinh ra từ quá trình quang hợp của cây xanh.
(e) Do nồng độ cao các muối của kim loại chì, thủy ngân,.. trong các nguồn nước.
Những nhận định đúng là
A. (a), (b), (c).
B. (b), (c), (e).
C. (a), (b), (d).
D. (b), (c), (d).
Câu 5: Cho 37,95 gam hỗn hợp gồm 2 muối $\mathrm{MgCO}_3$ và $\mathrm{RCO}_3$ vào $100 \mathrm{ml}$ dung dịch $\mathrm{H}_2 \mathrm{SO}_4$ loãng, thu được dung dịch $\mathrm{X}$, chất rắn $\mathrm{Y}$ và 1,12 lit $\mathrm{CO}_2$ (đkktc). Cô cạn dung dịch $\mathrm{X}$ thu được 4 gam muối khan. Nung chất rắn $\mathrm{Y}$ đến khối lượng không đổi thì thu được chất rắn $\mathrm{Z}$ và 4,48 lit $\mathrm{CO}_2$ (đkktc). Khối lượng chấn là
A. 26,95 gam.
B. $27,85 \mathrm{gam}$.
C. 29,15 gam.
D. 23,35 gam.
Câu 6: Hòa tan hết 26,43 gam hỗn hợp bột gồm $\mathrm{Mg}, \mathrm{Al}, \mathrm{Al}_2 \mathrm{O}_3$ và $\mathrm{MgO}$ bằng $800 \mathrm{ml}$ dung dịch hỗn hợp gồm $\mathrm{HCl} 0,5 \mathrm{M}$ và $\mathrm{H}_2 \mathrm{SO}_4 0,75 \mathrm{M}$ (vừa đủ). Sau phản úng thu được dung dịch $\mathrm{X}$ và 4,368 lit khi $\mathrm{H}_2$ (đktc). Cô cạn dung dịch $\mathrm{X}$ thu được $\mathrm{m}$ gam muối khan. Giá trị của $\mathrm{m}$ là
A. 98,98 .
B. 88,55 .
C. 100,52 .
D. 86,58 .
Câu 7: Cho các sơ đồ phản ứng sau:
$
\begin{aligned}
& \mathrm{X}_1+\mathrm{X}_2 \rightarrow \mathrm{X}_4+\mathrm{H}_2 \\
& \mathrm{X}_3+\mathrm{X}_4 \rightarrow \mathrm{CaCO}_3+\mathrm{NaOH} \\
& \mathrm{X}_3+\mathrm{X}_5+\mathrm{X}_2 \rightarrow \mathrm{Fe}(\mathrm{OH})_3+\mathrm{CO}_2+\mathrm{NaCl}
\end{aligned}
$
Các chất thích hợp với $\mathrm{X}_3, \mathrm{X}_4, \mathrm{X}_5$ lần lượt là
A. $\mathrm{Ca}(\mathrm{OH})_2, \mathrm{NaHCO}_3, \mathrm{FeCl}_3$.
C. $\mathrm{Na}_2 \mathrm{CO}_3, \mathrm{Ca}(\mathrm{OH})_2, \mathrm{FeCl}_3$.
B. $\mathrm{Na}_2 \mathrm{CO}_3, \mathrm{Ca}(\mathrm{OH})_2, \mathrm{FeCl}_2$.
D. $\mathrm{Ca}(\mathrm{OH})_2, \mathrm{NaHCO}_3, \mathrm{FeCl}_2$.
Câu 8: Hòa tan hoàn toàn hai chất rắn $\mathrm{X}, \mathrm{Y}$ (có số $\mathrm{mol}$ bằng nhau) vào nước thu được dung dịch $\mathrm{Z}$.
Tiến hành các thí nghiệm sau:
Thí nghiệm 1: Cho dung dịch $\mathrm{NaOH}$ dư vào $\mathrm{V} \mathrm{ml}$ dung dịch $\mathrm{Z}$, thu được $\mathrm{m}_1$ gam kết tủa. Thí nghiệm 2: Cho dung dịch $\mathrm{K}_2 \mathrm{CO}_3$ dư vào $\mathrm{V} \mathrm{ml}$ dung dịch $\mathrm{Z}$, thu được $\mathrm{m}_2$ gam kết tủa. Thí nghiệm 3: Cho dung dịch $\mathrm{AgNO}_3$ dư vào $\mathrm{V} \mathrm{ml}$ dung dịch $\mathrm{Z}$, thu được $\mathrm{m}_3$ gam kết tủa. Biết các phản ưng xảy ra hoàn toàn và $\mathrm{m}_1<m_2<m_3$. Trong số các cặp chất $(\mathrm{X}, \mathrm{Y})$ sau:
(a) $\mathrm{NaCl}, \mathrm{FeCl}_2$
(d) $\mathrm{Ca}\left(\mathrm{HCO}_3\right)_2, \mathrm{CaCl}_2$
(b) $\mathrm{NaNO}_3, \mathrm{BaCl}_2$
(c) $\mathrm{KCl}, \mathrm{Ba}\left(\mathrm{HCO}_3\right)_2$
Số cặp chất thỏa mãn là
(e) $\mathrm{NaHCO}_3, \mathrm{CaCl}_2$
A. 2.
B. 5 .
C. 4 .
D. 1 .
Câu 9. Thực hiện các thí nghiệm sau:
(a) Cho hỗn hợp $\mathrm{Cu}$ và $\mathrm{Fe}_3 \mathrm{O}_4$ (tỉ lệ mol tương ứng $2: 1$ ) vào dung dịch $\mathrm{HCl}$ (dư).
(b) Cho $0,2 \mathrm{~mol} \mathrm{Na}$ vào $100 \mathrm{ml}$ dung dịch chúa $0,2 \mathrm{~mol} \mathrm{CuSO}_4$.
(c) Cho hỗn hợp $\mathrm{Ba}$ và $\mathrm{NaHCO}_3$ (ti lệ mol $1: 1$ ) vào nước (dư).
(d) Đun nóng dung dịch chứa $\mathrm{NaHCO}_3, \mathrm{CaCl}_2$ (tỉ lệ mol 1:1).
(e) Cho dung dịch $\mathrm{BaCl}_2$ dư vào dung dịch $\mathrm{KHSO}_4$.
(f) Cho hỗn hợp gồm $0,15 \mathrm{~mol} \mathrm{Na}$ và $0,1 \mathrm{~mol} \mathrm{Al}$ vào nước dưr.
Sau khi các phản ứng xảy ra hoàn toàn, số thí nghiệm thu được dung dịch chứa hai chất tan là
A. 2.
B. 5 .
C. 4 .
D. 3 .
Câu 10: Tại một nhà máy hóa chất có sự cố, sau tiếng nổ lớn, một cột khi $\mathrm{X}$ màu vàng lục bốc lênn, ngay sau đó cột khí này từ từ rơi xuống và bao trùm lấy nhà máy. Trong một khoảng thời gian ngắn, cây cối quanh nhà máy khô héo và chuyển màu. Các công nhân cảm thấy ngạt thở, cuống họng khô rát, nhức đầu, chóng mặt, một số thì bị ói mửa và bất tinh. Người ta đã lấy mẫu $X$ nghiên cứu và cho các kết quả sau: (a) Khi cho khi $\mathrm{X}$ tác dụng hoàn toàn với 11,2 gam sắt thì thu được 25,4 gam muối.
(b) Khí $\mathrm{X}$ tan trong nước tạo thành dung dịch có khả năng tầy màu.
(c) Nhỏ dung dịch bạc nitrat vào dung dịch $\mathrm{X}$ thấy xuất hiện kết tủa trắng.
(d) Trong phòng thi nghiệm, có thể thu khí $\mathrm{X}$ bằng phương pháp đẩy nước.
(e) Khi $\mathrm{X}$ tác dụng với dung dịch $\mathrm{NaOH}$, đun nóng được dung dịch nước Gia-ven.
(f) Sục khí sunfurơ vào dung dịch $\mathrm{X}$ rồi nhỏ dung dịch bari clorua vào thấy có kết tủa trắng. Số nhận định đúng là
A. 2 .
B. 4 .
C. 3 .
D. 5 .
Câu 11. Hòa tan hoàn toàn 14,01 gam hỗn hợp gồm $\mathrm{Na}, \mathrm{Na}_2 \mathrm{O}, \mathrm{Ba}$ và $\mathrm{BaO}$ vào nước thu được 3,36 lít khí $\mathrm{H}_2$ (đktc) và dung dịch $\mathrm{X}$. Sục $\mathrm{V}$ lít khí $\mathrm{CO}_2$ (đktc) vào $\mathrm{X}$, thu được 1,97 gam kết tủa và dung dịch $\mathrm{Y}$. Cho từ từ dung dịch $\mathrm{HCl} 1 \mathrm{M}$ vào $\mathrm{Y}$, sự phụ thuộc thể tích khí $\mathrm{CO}_2$ (đktc) thoát ra và thể tích dung dịch $\mathrm{HCl} 1 \mathrm{M}$ được biểu diễn theo đồ thị sau:
Giá trị của V là
A. 5,376.
B. 4,480 .
C. 5,600 .
D. 4,256 .
Câu 12: Cho 8,654 gam hỗn hợp khí $\mathrm{Cl}_2$ và $\mathrm{O}_2$ tác dụng vừa đủ với $0,396 \mathrm{~mol}$ hônn hợp $\mathrm{Y}$ gồm $\mathrm{Mg}, \mathrm{Zn}$, Al thì thu được 23,246 gam hỗn hợp Z gồm muối clorua và oxit của $3 \mathrm{kim}$ loại. Cho $\mathrm{Z}$ phản ứng vừa đủ với $\mathrm{V} \mathrm{ml}$ dung dịch $\mathrm{HCl} 2 \mathrm{M}$ thì thu được dung dịch $\mathrm{T}$. Cho từ từ dung dịch $\mathrm{Ba}(\mathrm{OH})_2 2 \mathrm{M}$ vào $\mathrm{T}$ đến khi khối lượng kết tủa thu được lớn nhất thì cần vù̀a đủ $212 \mathrm{ml}$. Giá trị của $\mathrm{V}$ là
A. 780 .
B. 864 .
C. 390 .
D. 848 .
Câu 13: Nung nóng $\mathrm{m}$ gam hổn hợp $\mathrm{X}$ gồm $\mathrm{Zn}, \mathrm{Mg}, \mathrm{Al}$ và $\mathrm{Cu}$ trong $\mathrm{O}_2$ dư, thu được $(2 \mathrm{~m}-21,7)$ gam hỗn hợp $\mathrm{Y}$ gồm các oxit. Hòa tan hết $\mathrm{Y}$ bằng lượng vừa đủ dung dịch gồm $\mathrm{HCl} 2 \mathrm{aM}$ và $\mathrm{H}_2 \mathrm{SO}_4 \mathrm{aM}$, thu được dung dịch chứa 76,425 gam hỗn hợp muối trung hòa. Biết các phản úng xảy ra hoàn toàn. Giá trị của $\mathrm{m}$ là
A. 44,8 .
B. 24,5 .
C. 30,5 .
D. 22,3 .
Câu 14: Hòa tan hết 31,44 gam hỗn hơp $\mathrm{X}$ gồm $\mathrm{Fe}, \mathrm{FeO}, \mathrm{Fe}_2 \mathrm{O}_3$ và $\mathrm{Fe}_3 \mathrm{O}_4$ vào dung dịch $\mathrm{HCl}$ (dư), thu được $0,045 \mathrm{~mol} \mathrm{H}_2$ và dung dịch chứa $\mathrm{a}$ gam hỗn hợp muối. Mặt khác, hòa tan hoàn toàn $\mathrm{m}$ gam $\mathrm{X}$ trong dung dịch chứa $0,6 \mathrm{~mol} \mathrm{H}_2 \mathrm{SO}_4$ đặc, đun nóng, thu được dung dịch $\mathrm{Y}$ và $0,14 \mathrm{~mol} \mathrm{SO}_2$ (sản phẩm khử duy nhất của $\mathrm{H}_2 \mathrm{SO}_4$ đặc). Cho $250 \mathrm{ml}$ dung dịch hỗn hợp gồm $\mathrm{NaOH} 1 \mathrm{M}$ và $\mathrm{KOH} 1 \mathrm{M}$ vào $\mathrm{Y}$, sau khi phản ứng kết thúc thu được 16,05 gam kết tủa chi chứa 1 chất. Giá trị của a gần nhất với
A. 58,97 .
B. 39,32 .
C. 51,90 .
D. 31,19 .
Câu 15: Cho sơ đồ phản ứng sau:
(1) $(\mathrm{X})+\mathrm{HCl} \rightarrow\left(\mathrm{X}_1\right)+\left(\mathrm{X}_2\right)+\mathrm{H}_2 \mathrm{O}$
(5) $\left(\mathrm{X}_2\right)+\mathrm{Ca}(\mathrm{OH})_2 \rightarrow\left(\mathrm{X}_7\right)$
(2) $\left(\mathrm{X}_1\right)+\mathrm{NaOH} \rightarrow\left(\mathrm{X}_3\right)+\left(\mathrm{X}_4\right)$
(6) $\left(\mathrm{X}_7\right)+\mathrm{NaOH} \rightarrow\left(\mathrm{X}_8\right)+\left(\mathrm{X}_9\right)+\ldots$
(3) $\left(\mathrm{X}_1\right)+\mathrm{Cl}_2 \rightarrow\left(\mathrm{X}_5\right)$
(7) $\left(\mathrm{X}_8\right)+\mathrm{HCl} \quad \rightarrow\left(\mathrm{X}_2\right)+\ldots$
(4) $\left(X_3\right)+\mathrm{H}_2 \mathrm{O}+\mathrm{O}_2 \rightarrow\left(X_6\right)$
(8) $\left(X_5\right)+\left(X_9\right)+H_2 \mathrm{O} \rightarrow\left(X_4\right)+\ldots$
Biết $X_5$ có màu nâu đỏ, cho các nhận định sau:
(a) $X_7$ có khả năng tác dụng với dung dịch $\mathrm{HCl}$.
(b) $X_3$ không tan trong nước, màu nâu đỏ.
(c) Đốt cháy dây sắt trong oxi tạo ra $\mathrm{X}$.
(d) $X_8$ không tan trong nước nhưng tan trong nước bão hòa $\mathrm{CO}_2$.
(e) $X_2$ là sản phẩm của phản úng khi đốt nóng sắt trong khí clo.
Số nhận định đúng là
A. 2.
B. 5 .
C. 4 .
D. 3 .
Câu 16: Đặt hai cốc $\mathrm{A}$ và $\mathrm{B}$ chứa dung dịch $\mathrm{HCl}$ loãng (dùng dư) trên hai đĩa cân, cân ở trạng thái cân bằng. Thực hiện các thi nghiệm sau:
(b) Cho $1 \mathrm{~mol} \mathrm{Fe} \mathrm{vào} \mathrm{cốc} \mathrm{A}$ và $1 \mathrm{~mol} \mathrm{CaO}$ vào cốc $\mathrm{B}$.
(c) Cho $1 \mathrm{~mol} \mathrm{FeO}$ vào cốc $\mathrm{A}$ và $1 \mathrm{~mol} \mathrm{FeCO}_3$ vào cốc $\mathrm{B}$.
(d) Cho $1 \mathrm{~mol} \mathrm{Na}_2 \mathrm{~S}$ vào cốc $\mathrm{A}$ và $1 \mathrm{~mol} \mathrm{Al}(\mathrm{OH})_3$ vào cốc $\mathrm{B}$.
(e) Cho $1 \mathrm{~mol} \mathrm{FeS} \mathrm{vào} \mathrm{cốc} \mathrm{A}$ và $1 \mathrm{~mol} \mathrm{Fe}$ vào cốc $B$. Giả sử nước bay hơi không đáng kể, sau khi các phản ưng xảy ra hoàn toàn, số trường hợp cân trở lại vị trí cân bằng là
A. 2.
B. 4.
C. 5 .
D. 3 .
Câu 17: Cho a gam một muối halogenua của một kim loại kiềm tác dụng với $125 \mathrm{ml}$ dung dịch $\mathrm{H}_2 \mathrm{SO}_4$ đặc, nóng vừa đủ. Sau khi phản ứng xảy ra hoàn toàn, để nguội, thu được hỗn hợp sản phẩm $\mathrm{X}$ trong đó có một khí $\mathrm{Y}$ (mùi trúng thối). Cho toàn bộ khí $\mathrm{Y}$ tác dụng với dung dịch $\mathrm{Cu}\left(\mathrm{NO}_3\right)_2$ du thu được 14,4 gam kết tủa màu đen. Phần sản phẩm còn lại, làm khô thu được 237,6 gam chất rắn $\mathrm{T}$. Nung $\mathrm{T}$ đến khối lượng không đổi thu được 85,2 gam muối duy nhất. Biết các phản ứng xảy ra hoàn toàn. Giá trị của a là
A. 256.
B. 180 .
C. 190 .
D. 204 .
Câu 18: Hỗn hợp $X(\mathrm{Na}, \mathrm{K}, \mathrm{Ba})$ trong $\mathrm{X}$ có số $\mathrm{mol}$ của Ba bằng một nửa số $\mathrm{mol}$ của hỗn hơp. Cho $\mathrm{m}$ gam hỗn hợp $\mathrm{X}$ tan hết trong $\mathrm{H}_2 \mathrm{O}$, thu được dung dịch $\mathrm{Y}$ và khi $\mathrm{H}_2$. Cho toàn bộ khí $\mathrm{H}_2$ tạo ra đi qua một ống chứa $0,3 \mathrm{~mol} \mathrm{CuO}$ và $0,2 \mathrm{~mol} \mathrm{FeO} \mathrm{nung} \mathrm{nóng,} \mathrm{sau} \mathrm{phản} \mathrm{ứng} \mathrm{thu} \mathrm{được} \mathrm{33,6} \mathrm{gam} \mathrm{chất} \mathrm{rắn} \mathrm{trong} \mathrm{ống.} \mathrm{Đem}$ toàn bộ dung dich $\mathrm{Y}$ cho vào một dung dịch chứa $0,3 \mathrm{~mol} \mathrm{HCl}, 0,02 \mathrm{~mol} \mathrm{AlCl}_3$ và $0,05 \mathrm{~mol} \mathrm{Al}_2\left(\mathrm{SO}_4\right)_3$ thu được y gam kết tủa. Biết các phản ứng hoàn toàn. Giá trị của y là
A. 41,19 .
B. 52,30 .
C. 37,58 .
D. 42,75 .
Câu 19: Đốt cháy hoàn toàn 5 gam hỗn hợp $\mathrm{C}$ và $\mathrm{S}$ trong $\mathrm{O}_2$ vừa đủ thu được hỗn hợp $\mathrm{X}$ gồm $\mathrm{CO}_2$ và $\mathrm{SO}_2$. Dẫn $\mathrm{X}$ tù̀ tù qua $100 \mathrm{ml}$ dung dịch $\mathrm{Y}$ chứa $\mathrm{NaOH}$ và $\mathrm{KOH}$ đến phản úmg hoàn toàn thu được $\mathrm{V}_1 \mathrm{ml}$ dung dịch $\mathrm{Z}$ chi chúa $\mathrm{m}_1$ gam muối. Cho dung dịch nước vôi trong dư vào dung dịch $\mathrm{Z}$ thi thấy xuất hiện 27 gam kết tuia. Nếu dẫn $\mathrm{X}$ từ từ qua $150 \mathrm{ml}$ dung dịch $\mathrm{Y}$ đến phản ứng hoàn toàn thì thu được $\mathrm{V}_2 \mathrm{ml}$ dung dịch $\mathrm{T}, \mathrm{cô}$ cạn $\mathrm{T}$ thu được $\mathrm{m}_2$ gam rắn khan. Biết $\mathrm{m}_2-\mathrm{m}_1=8,645$ gam và khi trộn $2,5 \mathrm{~V}_1 \mathrm{ml}$ dung dịch $\mathrm{Z}$ với $\mathrm{V}_2 \mathrm{ml}$ dung dịch $\mathrm{T}$ thì dung dịch sau phản ứng chi chứa các muối trung hòa. Giá trị $\left(\mathrm{m}_1+\mathrm{m}_2\right)$ gần nhất vởi
A. 67 .
B. 64 .
C. 57.
Câu 20: Nung nóng $\mathrm{m}$ gam hỗn hợp gồm $\mathrm{Cu}$ và $\mathrm{Fe}$ (tỵ lệ mol 3:4) rồi cho một luồng khi $\mathrm{O}_2$ đí qua sau một thời gian thu đượ $(\mathrm{m}+0,64)$ g. một thời gian thu được $(\mathrm{m}+0,64)$ gam hỗn hợp rắn $\mathrm{X}$. Hòa tan hoàn toàn lượng $\mathrm{X}$ trên vào dung dịch $\mathrm{H}_2 \mathrm{SO}_4$ dặc, nóng, dư thu được dung dịch $\mathrm{Y}$ và $\mathrm{V}$ lít khi $\mathrm{SO}_2$ (Aktc, sản phẩm khử duy nhất). Cho dung dịch $\mathrm{Ba}(\mathrm{OH})_2$ dư vào $\mathrm{Y}$ thấy xuất hiện 75,02 gam kết tủa $\mathrm{Z}$. Lấy toàn bộ lượng $\mathrm{Z}$ trên nung tới khổi lượng không đồi thu được 71,78 gam chất rắn $\mathrm{T}$. Cho các phát biểu sau:
(a) Giá trị của $m$ là 8,23 .
(b) Giá trị của V là 3,136.
(c) Số mol $\mathrm{H}_2 \mathrm{SO}_4$ đã dùng ban đầu là $0,4 \mathrm{~mol}$.
(d) Số $\mathrm{mol} \mathrm{H}_2 \mathrm{SO}_4$ trong dung dịch $\mathrm{Y}$ là $0,06 \mathrm{~mol}$.
(e) \% khối lượng của $\mathrm{O}$ trong $\mathrm{Z}$ là $29,86 \%$.
Số phát biểu đúng là
A. 5.
B. 2 .
B. PHÀN TỰ LUẬ: $(10,0$ điểm).
Câu I $(l, 5$ điểm).
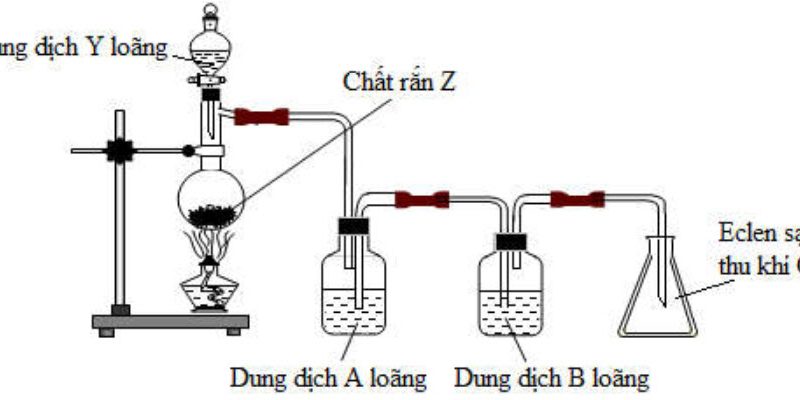
1. Cho sơ đồ thí nghiệm sau:
Viết các phương trình phàn úmg xáy ra. Biết chất rắn $\mathrm{Y}$ gồm: $\mathrm{CuO}, \mathrm{Al}_2 \mathrm{O}_3, \mathrm{MgO}_2 \mathrm{Fe}_3 \mathrm{O}_4, \mathrm{PbO}$.
2. Xác đính các chất $\mathrm{A}, \mathrm{B}, \mathrm{D}, . . \mathrm{M}$ trong sơ đồ các phản ưng sau và viết phương trinhh hơa họe đề hoản thành các phàn ưng đơ: (Biêt $A$ là hơp chất của $\mathrm{Na})$
a. $(\mathrm{A})+(\mathrm{B}) \longrightarrow(\mathrm{D})+\mathrm{H}_2 \mathrm{O}$
c. $(\mathrm{A})+(\mathrm{G}) \longrightarrow(\mathrm{H})+(\mathrm{B})+\mathrm{H}_2 \mathrm{O}$
b. $(\mathrm{A})+(\mathrm{E}) \longrightarrow(\mathrm{F})+\mathrm{CO}_2+\mathrm{H}_2 \mathrm{O}$
e. (A) $\longrightarrow$ (D) $+\mathrm{CO}_2+\mathrm{H}_2 \mathrm{O}$
d. $(\mathrm{A})+(\mathrm{I}) \longrightarrow(\mathrm{D})+(\mathrm{J})+\mathrm{H}_2 \mathrm{O}$
Câu II (I,5 điểm).
f. $(\mathrm{A})+(\mathrm{K}) \longrightarrow(\mathrm{L})+(\mathrm{M})+\mathrm{CO}_2+\mathrm{H}_2 \mathrm{O}$
1. Chất rùn $\mathrm{A}$ có sẫn trong tư nhiên dướ dạng nhiều loại khoáng khác nhau. Nung nóng $\mathrm{A} o ̛ 1100^{\circ} \mathrm{C}$ là phương pháp để sán xuát lương lớn chất $\mathrm{B}$. Cho $\mathrm{B}$ phản ưng vơii nước sê đưope chất $\mathrm{D}$ và tỏa nhiểu nhiệt. Trong phòng thí nghiêm, dung dịch nước của $\mathrm{D}$ được dùng để phát hiẹn khí $\mathrm{E}$, Khi $\mathrm{E}$ đưope sừ dụng trong rất nhiều loại nước giaii khát.
a. Viết các phương trình phàn úng thể hiện caic biến đới hóa họce ơ trên.
b. Khí $\mathrm{E}$ ơ trên cô nhiều ưng dụng trong công nghiêp, một trơng số đó là điều chế muối $\mathrm{F}$ (không bền) theo phương pháp Solvay: cho một lượng bằng nhau về sô mol cùa $\mathrm{NH}_3$ và khi $\mathrm{E}$ sục qua dung dịch natri clorua (nước biển) ờ nhiệt độ thấp. Sàn phẩm tao thành ngoài muối $\mathrm{F}$ còn có muối amoni clorua $\mathrm{NH}_4 \mathrm{Cl}$. Do it tan ở nhiệt độ thấp nên muối $\mathrm{F}$ sẽ két tủa. Viết phản ưng điều chế muối $\mathrm{F}$ theo phương pháp Solvay.
2. Cho các chất $\mathrm{X}, \mathrm{Y}, \mathrm{Z}, \mathrm{T}$ (đều bị phân hùy ở nhiêt độ cao) thớa mãn các tỉnh chất sau:
– X dùng làm bột nờ, tác dụng với dung dịch $\mathrm{HCl}$ họ̣̆c dung dịch $\mathrm{NaOH}$ dư, đun nóng đều sủi bọt khí.
Y có trong thành phần thuốc chữa đau dạ dày, tạo sản phẩm khí khi tác dụng với dung dịch ACl và tạo két tủa trắng với dung dịch $\mathrm{Ca}(\mathrm{OH})_2$.
– $Z$ thường được dùng để điều chế oxi trong phòng thí nghiệm.
– Nung $T$ thu được chất rắn $M$ dùng để khử trùng chuồng trại chăn nuôi, điều ché vôi sữa,.. Biết tổng khối lượng mol phân tử của $X, Y, Z, T$ là 421. Xác định các chát $X, Y, Z, T$, giaii thích và viét các phương trình phản ứng minh họa. Câu III (3,0 diếm).
1. Hòa tan hoàn toàn 21,24 gam hỗn hợp $\mathrm{A}$ gồm muối hidrocacbonat $\mathrm{X}$ và muối cacbonat $\mathrm{Y}$ vào nước thu được $200 \mathrm{ml}$ dung dịch $\mathrm{Z}$. Cho từ từ $200 \mathrm{ml}$ dung dịch $\mathrm{KHSO}_4 0,3 \mathrm{M}$ và $\mathrm{HCl} 0,45 \mathrm{M}$ vào $200 \mathrm{ml}$ dung dịch $\mathrm{Z}$ thu được 1,344 lít khí $\mathrm{CO}_2$ (dktc) và dung dịch $\mathrm{T}$. Cho dung dịch $\mathrm{Ba}(\mathrm{OH})_2$ dư vào $\mathrm{T}$, thu được 49,44 gam kết tủa. Biết $\mathrm{X}$ là muối của kim loại kiềm. Xác định công thức phân tử của $\mathrm{X}$, $\mathrm{Y}$ và tính phàn trăm khối lượng mỗi muối trong $\mathrm{A}$.
2. $\mathrm{X}$ là một muối nhôm khan, $\mathrm{Y}$ là một muối vô cơ khan. Hòa tan a gam hổn hợp $\mathrm{X}$ và $\mathrm{Y}$ ( $\mathrm{X}, \mathrm{Y}$ có cùng số $\mathrm{mol})$ vào $200 \mathrm{ml}$ nước được dung dịch $\mathrm{A}$. Cho dung dịch $\mathrm{Ba}(\mathrm{OH})_2$ dư vào dung dịch $\mathrm{A}$ thu được c dung dịch $\mathrm{B}$, khí $\mathrm{D}$ và 7,689 gam kết tủa $\mathrm{E}$ ( $\mathrm{E}$ không tan trong axit mạnh). Trung hòa $\mathrm{B}$ bằng dung dịch $\mathrm{HNO}_3$ dư, sau đó thêm $\mathrm{AgNO}_3$ vào thì thấy xuất hiện kết tủa màu trắng bị đen dần khi để ngoài ánh sáng. Mặt khác, khi thêm $\mathrm{Ba}(\mathrm{OH})_2$ vào $\mathrm{A}$ cho đến khi đạt lượng kết tủa lớn nhất (kết tủa $\mathrm{F}$ ) thi dừng lại. Nung $\mathrm{F}$ tới khối lượng không đổi thu được 9,372 gam chất rắn.
a. Xác định công thức của các muối $X, Y$.
b. Tính a và nồng độ mol $/ \mathrm{l}$ của các chất trong dung dịch $\mathrm{A}$.
Câu IV (2,0 diểm).
1. Cho 1,2 gam hỗn hợp $\mathrm{X}$ gồm $\mathrm{Fe}$ và $\mathrm{Cu}$ tác dụng với $100 \mathrm{ml}$ dung dịch $\mathrm{AgNO}_3 \times \mathrm{mol} /$. Sau khi các phản úng xảy ra hoàn toàn thu được dung dịch $\mathrm{Y}$ và 3,94 gam chất rắn $\mathrm{Z}$. Cho $\mathrm{Y}$ tác dụng với dung dịch $\mathrm{NaOH}$ dư, lọc kết tủa, nung trong không khí đến khối lượng không đổi thu được 1,4 gam chất rấn $\mathrm{T}$.
a. Tính phần trăm khối lượng các kim loại trong hỗn hợp X.
b. Tính $x$.
2. Hạt mắc-ca (macadamia) rất nối tiếng vì giá trị dinh dưỡng và sự thơm ngon của nó. Để cây phát triển tốt thì giai đoạn bón thúc cần dùng phân bón thích hợp là NPK $4.12 .7$ (kí hiệu này cho biết tỉ lệ khối lượng các thành phần của $\mathrm{N}, \mathrm{P}_2 \mathrm{O}_5, \mathrm{~K}_2 \mathrm{O}$ trong phân bón).
a. Có ba mẫu phân bón amoni sunfat, canxi đihiđrophotphat và kali clorua. Để có loại phân bón NPK 4.12.7 phải trộn ba mẩu phân bón theo tỉ lệ khối lượng nào?
b. Nêu cách nhận biết ba mẫu phân bón trên đựng trong các lọ riêng biệt bằng một hóa chất duy nhất. Viết phương trình phản ưng minh họa.
Câu V (2,0 điểm).
Hỗn hơp $\mathrm{X}$ gồm: $\mathrm{MCO}_3, \mathrm{Fe}_x \mathrm{O}_y, \mathrm{FeCO}_3$ (với $\mathrm{M}$ là kim loại hóa trị II). Hòa tan $\mathrm{m}$ gam $\mathrm{X}$ cần đùng vù̀a đù $480 \mathrm{ml}$ dung dịch $\mathrm{HCl} 1 \mathrm{M}$. Mặt khác, hòa tan $\mathrm{m}$ gam $\mathrm{X}$ trong dung dịch $\mathrm{H}_2 \mathrm{SO}_4$ dặc, nóng, dư thu được dung dịch $\mathrm{Y}$ và 3,696 lit hỗn hợp khi $\mathrm{Z}$ (đkte). Cho $\mathrm{Y}$ tác dụng với dung dịch $\mathrm{KOH}$ dư thu được 19,53 gam kết tủa. Nung kết tủa này ngoải không khi đến khối lượng không đổi thu được 14,4 gam chất rắn $\mathrm{E}$ gồm 2 oxit kim loại. Dẫn từ từ 8,96 lít khí $\mathrm{CO}$ (dktc) qua 14,4 gam $\mathrm{E}$, nung nóng thu được hỗn hợp khi $\mathrm{T}$ có tỷ khối so với $\mathrm{H}_2$ là 18,5 . Biết các phản ưng xảy ra hoàn toàn và $\mathrm{SO}_2$ là sản phẩm khừ duy nhất cùa $\mathrm{H}_2 \mathrm{SO}_4$ đặc.
a. Viết các phương trình phản úng xảy ra.
b. Xác định công thức phân tử của $\mathrm{MCO}_3, \mathrm{Fe}_{\mathrm{x}} \mathrm{O}_y$ và tính $\mathrm{m}$.
Có thể bạn quan tâm: Đề thi vào 10 Chuyên Hóa ĐăkLăk– Năm học 2020 – 2021