Đề thi HSG Hoá 9 Tỉnh Nghệ An – Năm học 2022 – 2023
Đề thi HSG Hoá 9 Tỉnh Nghệ An – Năm học 2022 – 2023


Z/ 1 8upr
SƠ GIÁO DƯC VȦ ĐẢO TẠO
KỲ THI CHOQNHQC SINH GIỎI TỈNH LỚP 9
NÄM HOC $2022-2023$
Môn thi: HÔA HQ̣C – Bảng B
Thời gian làm bài 150 phút (không kể thời gian giao đề)
Cho biết:
– Nguyên từ khối của các nguyên tố: $\mathrm{H}=1 ; \mathrm{C}=12 ; \mathrm{N}=14 ; \mathrm{O}=16 ; \mathrm{Na}=23 ; \mathrm{Mg}=24 ; \mathrm{Al}=27$;
$\mathrm{P}=31 ; \mathrm{S}=32 ; \mathrm{Cl}=35,5 ; \mathrm{K}=39 ; \mathrm{Ca}=40 ; \mathrm{Fe}=56 ; \mathrm{Cu}=64 ; \mathrm{Zn}=65 ; \mathrm{Br}=80 ; \mathrm{Ag}=108 ; \mathrm{Ba}=137$.
– Các thể tích khí được quy về đo ở điều kiện tiêu chuẩn.
Câu 1. (3 điểm)
1. Viết phương trình hóa học của các phản ứng xảy ra trong các quá trình sau:
+ Dùng dung dịch $\mathrm{Ca}(\mathrm{OH})_2$ dư để loại bỏ $\mathrm{SO}_2, \mathrm{CO}_2$ trong khí thải công nghiệp.
+ Dùng dung dịch $\mathrm{NaHCO}_3$ để rửa vết bỏng do $\mathrm{NaOH}$ hoặc $\mathrm{H}_2 \mathrm{SO}_4$.
+ Nung đá vôi $\left(\mathrm{CaCO}_3\right)$ dùng để sản xuất vôi.
+ Dùng dung dịch $\mathrm{NaOH}$ để hòa $\tan \mathrm{Al}_2 \mathrm{O}_3$ trong quặng bôxit (trong quá trình sản xuất nhôm)
2. Nêu hiện tượng và viết phương trình hóa học xảy ra trong các thí nghiệm sau:
+ Cho dung dịch $\mathrm{BaCl}_2$ vào dung dịch $\mathrm{Na}_2 \mathrm{SO}_4$.
$+$ Nung nóng $\mathrm{Cu}(\mathrm{OH})_2$ trên ngọn lửa đèn cồn.
+ Sục $\mathrm{CO}_2$ dư vào dung dịch muối natri aluminat.
Câu 2. ( 3 điểm)
Viết phương trình hóa học của phản ứng thực hiện các sơ đồ chuyển hóa sau:
a. $\mathrm{Al} \longrightarrow \mathrm{Al}_2 \mathrm{O}_3 \longrightarrow \mathrm{AlCl}_3 \longrightarrow \mathrm{Al}(\mathrm{OH})_3 \longrightarrow \mathrm{NaAlO}_2 \longrightarrow \mathrm{Al}(\mathrm{OH})_3 \longrightarrow \mathrm{Al}_2 \mathrm{O}_3$
b. $\mathrm{Fe} \stackrel{\jmath}{\longrightarrow} \mathrm{FeCl}_2 \longrightarrow \underset{2}{\longrightarrow} \mathrm{Fe}(\mathrm{OH})_2 \longrightarrow \underset{2}{\longrightarrow} \mathrm{Fe}(\mathrm{OH})_3 \longrightarrow \mathrm{Fe}_2 \mathrm{O}_3 \longrightarrow \mathrm{FeCl}_3 \longrightarrow \mathrm{FeCl}_3$
Câu 3. (3 điểm)
1. Tiến hành các thí nghiệm: Nhiệt phân $\mathrm{KMnO}_4$ thu được khi $\mathrm{A}$; cho dung dịch $\mathrm{HCl}$ đặc vào $\mathrm{MnO}_2$ đun nóng thu được khí $\mathrm{B}$; cho $\mathrm{Cu}$ vào dung dịch $\mathrm{H}_2 \mathrm{SO}_4$ đặc nóng thu được khí $\mathrm{C}$; cho $\mathrm{NH}_4 \mathrm{HCO}_3$ vào dung dịch $\mathrm{NaOH}$ thu được khí $\mathrm{D}$; cho hỗn hợp $\mathrm{A}$ với $\mathrm{C}$ đi qua xúc tác $\mathrm{V}_2 \mathrm{O}_5$ đun nóng; trộn khí $\mathrm{B}$ với khí $\mathrm{D}$; nung nóng hỗn hợp $\mathrm{A}$ với $\mathrm{D}$. Xác định các khí $\mathrm{A}, \mathrm{B}, \mathrm{C}, \mathrm{D}$ và viết phương trình hóa học của phản ứng trong các thí nghiệm trên.
2. Hãy cho biết:
+ Tại sao không nên đốt than tổ ong trong phòng kín để sưởi ấm vào mùa đông ? Viết phương trình hóa học xảy ra.
+ Úng dụng dùng để dập tắt các đám cháy dựa vào tính chất nào của $\mathrm{CO}_2$ ?
Câu 4. (4 điểm)
1. Hòa tan hoàn toàn 12 gam hỗn hợp $\mathrm{X}$ gồm $\mathrm{Fe}$ và kim loại $\mathrm{Mg}$ trong 175 gam dung dịch $\mathrm{HCl}$ $14,6 \%$, thu được 6,72 lít khí $\mathrm{H}_2$ và dung dịch $\mathrm{Y}$.
a. Viết phương trình phản ứng xảy ra và tính phần trăm khối lượng các kim loại trong $X$.
b. Tính nồng độ phần trăm các chất tan trong $\mathrm{Y}, \quad 10,22 ; 10,7,64 ; 1,95$
2. Hỗn hợp $\mathrm{X}$ gồm $\mathrm{CuO}$ và $\mathrm{Fe}$. Hòa tan 9,6 gam $\mathrm{X}$ trong dung dịch $\mathrm{H}_2 \mathrm{SO}_4$ đặc, nóng, dư thu được a mol $\mathrm{SO}_2$. Mặt khác, cho 9,6 gam $\mathrm{X}$ vào $110 \mathrm{ml}$ dung dịch $\mathrm{HCl} 2 \mathrm{M}$ thu được dung dịch $\mathrm{Y}$ chỉ chứa hai muối và còn lại 2,56 gam một kim loại không tan. Biết các phản ứng xảy ra hoàn toàn.
a. Viết phương trình hóa học các phản ứng xảy ra.
b. Tính phần trăm khối lượng mỗi chất trong $\mathrm{X}$ và giá trị a.
Câu 5. (4 điểm)
1. Một loại phân bón $\mathrm{NPK}$ chứa $\mathrm{NH}_4 \mathrm{NO}_3,\left(\mathrm{NH}_4\right)_2 \mathrm{HPO}_4, \mathrm{KCl}$ và các tạp chất không chứa nguyên tố $\mathrm{N}, \mathrm{P}, \mathrm{K}$. Trên bao bì của loại phân bón $\mathrm{NPK}$ này có ghi các chữ số $\mathbf{1 5 . 2 0 . 8}$. Tính phần trăm khối lượng các chất $\mathrm{NH}_4 \mathrm{NO}_3,\left(\mathrm{NH}_4\right)_2 \mathrm{HPO}_4, \mathrm{KCl}$ trong loại phân bón $\mathrm{NPK}$ ở trên.
2. Cho 5,4 gam $\mathrm{Al}$ tác duung vừa đủ với $\mathrm{V}$ lít hỗn hơp khi $\mathrm{X}$ gồm $\mathrm{Cl}_2$ và $\mathrm{O}_2$ thu được 15,7 gam chất rắn. Viết phương trình hóa học các phản ứng xảy ra và tính $\mathrm{V}$.
3. Cho 9,0 gam muối $X$ (khan) tác dunng với dung dịch $\mathrm{H}_2 \mathrm{SO}_4$ loãng, dư, thu được 0,09 mol khi $\mathrm{CO}_2$.
a. Xác định công thức phân tử của $X$.
b. Hấp thụ hoàn toàn $0,09 \mathrm{~mol} \mathrm{CO}_2$ ở trên vào dung dịch chứa $\mathrm{X} \mathrm{mol} \mathrm{Ba}(\mathrm{OH})_2$ thu đưực $2 \mathrm{~m}$ gam kết tủa và dung dịch $\mathrm{Y}$. Cho $15 \mathrm{ml}$ dung dịch $\mathrm{NaOH} 1 \mathrm{M}$ vào $\mathrm{Y}$ thu được $\mathrm{m}$ gam kêt tưa. Tính giá trị $x$ và $m$.
Câu 6. (3 điểm)
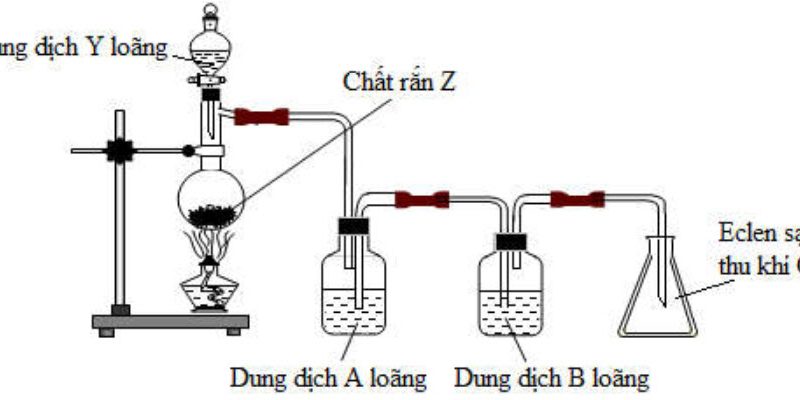
Thí nghiệm điều chế và thu khí $\mathrm{X}$ được mô tả như hình vẽ bên.
+ Xác định $\mathrm{X}$ và viết phương trình hóa học.
+ Hãy cho biết chất $Y$ và vai trò của bông tẩm dung dịch chất Y. Viết phương trình hóa học (nếu có). + Cho biết phương pháp thu khí $\mathrm{X}$ và phương pháp này dựa vào tính chất nào của $\mathrm{X}$ ?
+ Làm thế nào để biết khí $\mathrm{X}$ đầy bình thu ?
+ Trình bày cách làm khô khí $\mathrm{X}$ sinh ra ở thí nghiệm.
+ Nêu vài ứng dụng của khí $\mathrm{X}$ mà em biết.
HÉT
(Thí sinh được sủ̉ dụng bảng tuần hoàn các nguyên tố hóa học, cán bộ xem thi không giải thích gì thêm)
Có thể bạn quan tâm: Đề thi Chuyên Hóa ĐăkLăk– 2021