Đề thi HSG Hóa 9 – Tỉnh Tây Ninh– Năm học 2021 – 2022
Đề thi HSG Hóa 9 – Tỉnh Tây Ninh– Năm học 2021 – 2022
Bài 1. (2,5 điểm)
Trong phòng thí nghiệm người ta tiến hành một số thí nghiệm sau
Thí nghiệm 1: Sục từ từ tới dư khí $\mathrm{SO}_{2}$ vào dung dịch $\mathrm{KMnO}_{4}$
Thí nghiệm 2: Cho $\mathrm{K}_{2} \mathrm{CO}_{3}$ vào dung dịch $\mathrm{AlCl}_{3}$.
Thí nghiệm 3: Cho từ từ tới dư $\mathrm{CO}_{2}$ vào dung dịch $\mathrm{Ca}(\mathrm{OH})_{2}$.
Thí nghiệm 4: Cho từ từ tới dư $\mathrm{Ba}(\mathrm{OH})_{2}$ vào ống nghiệm đựng $\mathrm{Al}_{2}\left(\mathrm{SO}_{4}\right)_{3}$
Nêu hiện tượng viết các phương trình hản ứng xảy ra cho từng thí nghiệm trên
Bài 2. (2.0 điểm)
2.1. Cho các chất hữu cơ sau: etillen, axetilen, glucozo, saccarozo, chất béo và tinh bột. được kí hiệu ngẫu nhiên là $\mathrm{A}, \mathrm{B}, \mathrm{C}, \mathrm{D}, \mathrm{E}$ và $\mathrm{F}$ biết rằng:
– Chất $\mathrm{A}$ có phản ứng tráng gương.
– Chất $\mathrm{B}$ có phản ứng thủy phân, không tan trong nước ở nhiệt độ thường, không có trong cơ thể động vật
– Chất $\mathrm{C}$ tác dụng với dung dịch $\mathrm{AgNO}_{3} / \mathrm{NH}_{3}$ tạo kết tủa
– Chất $\mathrm{D}$ có phản ứng thủy phân không tạo ra chất $\mathrm{A}$
Xác định các chất $A, B, C, D$ và viết hương trình phản ứng đẫ nêu.
2.2. Xác định các chất $X, Y$ và viết các phương trình phản ứng theo chuỗi chuyển hóa sau
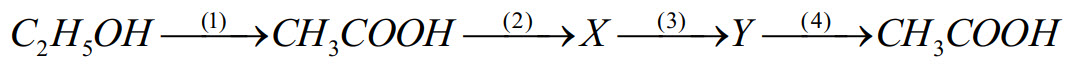
Bài 3: (1,5 điểm)
Cho 26,1 gam $\mathrm{MnO}_{2}$ vào dung dịch $\mathrm{HCl}$ đặc nóng dư. Khí clo thoát ra cho tác dụng hết với kim loại $\mathrm{R}$ thu được 30,9 gam hỗn hợp chất rắn $X$. cho $\mathrm{X}$ vào dung dịch $\mathrm{AgNO}_{3}$ dư thu được 107,7 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn, xác định tên kim loại $\mathrm{R}$.
Bài 4.(2.0 điểm)
4.1. Chia 11,52 gam hỗn hợp $\mathrm{X}$ gồm axit axetic và ancol etylic thành hai phần bằng nhau
Cho phần 1 tác dụng với $\mathrm{Na}$ dư thu được 1,232 lít $\mathrm{H}_{2}$ (đktc). Đun phần 2 với $\mathrm{H}_{2} \mathrm{SO}_{4}$ đặc thu được $\mathrm{m}$ gam este với hiệu suất $80 \%$. Tính giá trị của $\mathrm{m}$.
4.2. Đốt chay hoàn toàn $\mathrm{V}$ lít hợp chất hữu cơ $\mathrm{A}$ cần $\mathrm{V}$ lít $\mathrm{O}_{2}$ sinh $\mathrm{ra} \mathrm{V}$ lít $\mathrm{CO}_{2}$ và $\mathrm{V}$ lít hơi nước. xác định CTPT của $\mathrm{A}$, biết các thể tích đo ở cùng điều kiện nhiệt độ áp suất.
Bài 5. (2.0 điểm)
5.1. Cho $\mathrm{m}$ gam hỗn hợp $\mathrm{X}$ gồm nhôm và đồng tác dụng hết với Clo thu được $\mathrm{n}$ gam muối . Cũng cho $\mathrm{m}$ gam natri tác dụng với clo thu được $\mathrm{n}$ gam muối. Tính phần trăm khối lượng của nhôm trong X.
5.2. Hòa $\tan 0,4$ gam $\mathrm{SO}_{3}$ vào a gam dung dịch $\mathrm{H}_{2} \mathrm{SO}_{4} 10 \%$ thì thu được dung dịch $\mathrm{H}_{2} \mathrm{SO}_{4} 12,25 \%$. Tính giá trị của $a$.
Bài 6. (1,5 điểm)
Đốt cháy hoàn toàn 0,06 mol hỗn hợp khí A gồm C2H2 và một anken thu được 0,16 mol CO2 và 0,12 mol $\mathrm{H}_{2} \mathrm{O}$. mặt khác cho $\mathrm{m}$ gam hỗn hợp khí $\mathrm{A}$ lội qua dung dịch $\mathrm{Br}_{2}$ dư thì có 0,05 mol $\mathrm{Br}_{2}$ tham gia phản ứng.
a. Tìm CTPT của anken
b. Tính giá trị của $\mathrm{m}$.
Bài 7. (2,0 điểm)
7.1. Cho 8,42 gam hỗn hợp $\mathrm{A}$ gồm $\mathrm{Na}_{2} \mathrm{CO}_{3}, \mathrm{NaOH}, \mathrm{CaCO}_{3}, \mathrm{Ca}(\mathrm{OH})_{2}$ tác dụng với dung dịch $\mathrm{HCl}$ dư thu được 0,672 lít khí $\mathrm{CO}_{2}$ (đktc) và dung dịch $\mathrm{B}$. cô cạn dung dịch $\mathrm{B}$ thu được 4,68 gam muối $\mathrm{NaCl}$ và $\mathrm{m}$ gam muối $\mathrm{CaCl}_{2}$. Tính giá trị của $\mathrm{m}$.
7.2. Đem hòa tan hoàn toàn 39,4 gam hỗn hợp $\mathrm{X}$ gồm $\mathrm{MgO}, \mathrm{FeO}, \mathrm{CuO}$ và $\mathrm{ZnO}$ vào dung dịch $\mathrm{HCl}$ vừa đủ, sau phản ứng thu được dung dịch $Y$. cô cạn dung dịch $\mathrm{Y}$ thu được $\mathrm{m}$ gam chất rắn khan. Mặt khác hòa tan cũng lượng $\mathrm{X}$ như trên vào $\mathrm{H}_{2} \mathrm{SO}_{4}$ loãng vừa đủ thu được dung dịch $\mathrm{Z}$, cô cạn $\mathrm{Z}$ thu được $(\mathrm{m}+12,5)$ gam chất rắn khan. Tính giá trị của $\mathrm{m}$
Bài 8 (2.0 điểm)
Đốt cháy hoàn toàn a gam chất béo $\mathrm{Y}$ cần 35,84 lít $\mathrm{O}_{2}$ (đktc) dẫn toàn bộ sản phẩm cháy vào dung dịch $\mathrm{Ca}(\mathrm{OH})_{2}$ dư thu được 114 gam kết tủa, đồng thời khối lượng dung dịch giảm 45,12 gam. Nếu cho a gam $\mathrm{Y}$ tác dụng vừa đủ với dung dịch $\mathrm{NaOH}$ thu được $\mathrm{b}$ gam muối
a. Tính giá trị của $a, b$.
b. Tính khối lượng xà phòng thu được từ $\mathrm{b}$ gam muối trên.. biết muối của axit béo chiếm $60 \%$ khối lượng xà phòng.
Bài 9 (2.0 điểm)
Nung 24,48 gam hỗn hợp $\mathrm{X}$ gồm $\mathrm{Fe}, \mathrm{Al}, \mathrm{Fe}_{3} \mathrm{O}_{4}$ trong điều kiện không có không khí đến khi hản ứng xảy ra hoàn toàn thu được hỗn hợp $Y$. chia $Y$ thành hai phần bằng nhau
– Phần 1 tác dụng vừa đủ với $240 \mathrm{ml}$ dung dịch $\mathrm{KOH}$ 0,5 $\mathrm{M}$ thu được $2 \mathrm{a} \mathrm{mol} \mathrm{H}_{2}$.
– Phần 2 tác dụng với dung dịch $\mathrm{H}_{2} \mathrm{SO}_{4}$ loãng dư thu được $5 \mathrm{a}$ mol $\mathrm{H}_{2}$ và dung dịch chứa $\mathrm{m}$ gam mû́íi. Tính giá trị của $\mathrm{m}$
Bài 10.(2.5 điểm)
Cho 5,6 lít(đktc) hỗn hợp khí và hơi $\mathrm{X}$ gồm $\mathrm{C}_{2} \mathrm{H}_{6} \mathrm{O}, \mathrm{C}_{3} \mathrm{H}_{6}$ (propilen), $\mathrm{C}_{2} \mathrm{H}_{2}$ vừa đủ làm mất màu hoàn coann $100 \mathrm{ml}$ dung dịch nước $\mathrm{Br}_{2} 2 \mathrm{M}$. mặt khác đốt cháy hoàn toàn 5,05 gam hỗn hợp X rồi hấp thụ toàn bôِ. sản phẩm cháy vào $200 \mathrm{ml}$ dung dịch $\mathrm{NaOH}$ thì thu được dung dịch $\mathrm{Y}$ chứa 27,4 gam muối. lấy $1 / 10$ dung dịch Y tác dụng với dung dịch $\mathrm{BaCl}_{2}$ dư thu được 1,97 gam kết tủa.
a. Tính nồng độ mol dung dịch $\mathrm{NaOH}$.
b. Tính phần trăm khối lượng của mỗi chất trong hỗn hợp X.
(Cho: $H=1 ; C=12 ; N=14 ; O=16 ; N a=23 ; M g=24 ; A l=27 ; \mathrm{Br}=80 ; P=31 ; \mathrm{S}=32, \mathrm{Cl}=35,5$;
$
K=39 ; C a=40 ; \mathrm{Fe}=56 ; \mathrm{Cu}=64 ; \mathrm{Zn}=65 ; \mathrm{Mn}=55 ; \mathrm{Ag}=108 ; I=127 ; \mathrm{Ba}=137 ; \mathrm{He}=4)
$